前言
鑑於現屆政府有意藉著《再生醫療三法》的施行來推動台灣生技產業的發展。近來,衛福部次長石崇良在經濟日報主辦的「生技產業論壇:生醫產業疫後新戰略」上談到以下五個重點:(1)寄望台灣在疫後能找到生醫發展的利基;(2)建立32個生物資料庫供作產、學、研等發展再生醫療之用;(3)公告《再生醫療三法》(以下簡稱「再生三法」)(即《再生醫療發展法》、《再生醫療施行管理條例》、《再生醫療製劑管理條例》),加速核准細胞治療方法之上市;(4)推動遠距離醫療以及(5)公布醫療機構電子病歷製作與管理辦法。[1]目前將在2021年12月預告修法、60天內徵詢各界意見,明年1至2月完成修訂,提交立法院審議。[2]取代現有的《特定醫療技術檢查檢驗醫療儀器施行或使用管理辦法》(下稱「特管辦法」)。該「特管辦法」是由醫療法第62條第2項授權主管機關制定。依據Research and Markets的預估,全球再生醫療市場在2020至2030年間的年均複合成長率將達到13.99%,市場規模為870.3億美元(當中包括580億美元之細胞製劑與細胞治療藥品、200億美元之組織工程、64億美元之基因治療產品以及26億美元之血漿產品。[3]基此,本文想藉著「再生三法」的立法推動工作,發現隱含其中的台灣生技產業趨勢。
第一章 生技產業的大未來
根據經濟部工業局對「生物技術」的定義,乃指運用分子生物學、細胞生物學、免疫學、基因體學及蛋白質體學等生命科學知識與基因工程、蛋白質工程、細胞工程與組織工程等技術為基礎,進行研發、製造或提升產品品質,以改善人類生活品質的科學技術。[4]至於法律上定義,係依《生技醫藥產業發展條例修正草案》(現行的《生技新藥產業發展條例》)(以下簡稱「生醫發展條例草案」)第4條「指用於人類與動植物用之新藥、新劑型製劑、高風險醫療器材、再生醫療、精準醫療、數位醫療及其他策略生技醫藥產品之產業。」與傳統產業相比,生技產業主要有以下特性:(1)高資本密集、高風險和產品開發期長;(2)屬高度立法監管場域,產品上市一般需經過屬地的審查機構的試驗;(3)屬知識與技術密集之整合性科技;(4)以全球市場為導向的專業化產業鏈;(5)產業發展較不受景氣循環的影響;(6)可提供更加優化之結合資通訊產業者的醫療保健服務。[5]唯若單以「應用層面」而言,又可分為以「製藥」為主的製藥產業與以「醫材」及「療養」為主的「醫療器材產業」及「健康福祉產業」。[6]晚近,以「再生醫療」為產業利基的新應用範圍日益蓬勃,係指利用細胞(分為同種同體、同種異體和異種異體)或組織製品(乃透過組織工程,利用細胞或組織所生成),以及具生物可相容性提供細胞生長之生醫材料、替換或修復人體組織或器官的功能。[7]基此,依據Market and Markets公司的研究報告指出,2018年市場規模為105億美元,預估2022年全球再生醫療市場將達到253億美元,其2018~2022年的複合年成長率達到24.6%。[8]
第一節 供人類使用之新藥
所謂「供人類使用之新藥」,依據藥事法第7條規定,係本法所稱新藥,係指經衛福部審查認定屬新成分、新療效複方或新使用途徑製劑之藥品。從新藥的研發到上市,分為非臨床試驗的藥物發現、四期的臨床試驗(一期為針對少數受試者的確認人體安全使用劑量範圍;二期為針對少數病患確認藥物療效;三期為針對大規模受試者的確認藥物的安全性為目的的試驗;四期則為上市後的持續監視)、上市申請、量產後監控和正式上市;因此,新藥從研發到上市,是一個極耗成本、資源的過程。 [9]
第二節 新藥和新劑型製藥
依生醫產業發展條例草案第4條規定,是指經衛福部審定屬新成分、新療效複方或新使用途徑製劑,及新劑型製劑之藥品。基此,由於是供人類使用之緣故,主管機關對新藥上市程序有較嚴格的把關機制。例如根據藥事法第39條第1項規定,製造、輸入藥品者,應向衛福部主管單位申請查驗登記,經核准發給藥品許可證後,始得製造或輸入。又,同條第4項亦規定藥品查驗登記申請應依「藥品查驗登記審查準則」辦理,係規定各項藥品查驗登記應注意與遵循之事宜。另外,為有效運用審查資源以增進民眾用藥可近性,衛福部亦公告多項相關審查機制,以期使新藥加速上市,促進公共利益。
第三節 高風險醫療器材
依生醫產業發展條例草案第4條規定,是指經衛福部審定屬第三等級之醫療器材(屬高風險醫療器材,例如人工牙根、玻尿酸植入物及角膜塑型片等)或須經臨床試驗始得核准之第二等級之醫療器材(屬中風險醫療器材,例如隱形眼鏡、血壓計及血糖計等)。
第四節 再生醫療
依生醫產業發展條例草案第4條規定,是指將細胞、基因用於人體構造、功能之重建或修復,以達到治療或預防為目的,並經衛福部審定之藥物、產品或技術。所謂「再生醫療產業」[10],主要由上游、中游及下游的產業鏈構成,旨在製作具有功能與生命性之身體器官組織,用於修復或是替換身體內因老化、生病、受損所造成不健康之器官和組織,或以其他的方式刺激體內組織或器官再生。前述上游廠商主要負責幹細胞收集與保存,而中游廠商從事各種類幹細胞開發,至於下游廠商則負責臨床實驗、移植技術及疾病治療;事實上,再生醫療有別於現存於醫學界的治療醫學與預防醫學之概念,因此又被稱為「第3類醫學」,乃主要包括組織工程與幹細胞療法兩大領域。
| 公司/機構 | 產品 | 上市櫃 |
| 長春藤生命科學 | 細胞相關技術的研發及應用 | -/- |
| 長聖國際生技 | 細胞新藥研發 | 上櫃(6712) |
| 尖端先進生醫 | 細胞保存及治療應用 | 上市(4186) |
| 光麗生醫 | 以細胞治療臨床應用為主要發展,提供脂肪間質幹細胞、免疫細胞儲存、臍帶血、臍帶幹細胞儲存服務與應用發展之公司。 | 上市(6431) |
| 三顧生醫 | 開發食道及膝蓋軟骨相關產品 | 上櫃(3224) |
| 基亞生物科技 | 新藥臨床開發、創新生物醫藥研發平台、分子檢測、細胞培養疫苗科技、學名藥生產行銷等多項事業。 | 上櫃(3176) |
| 訊聯生技 | 提供多項細胞、基因、檢測、醫美保養品等產品技術 | 上櫃(1784) |
| 台寶生醫 | 致力於細胞藥物的開發與運用,透過專利擁有的人體間葉幹細胞擴增技術,針對心血管疾病、骨科疾病、免疫及癌症等疾病,為患者提供創新的治療方式或藥品。 | 否 |
| 博晟生醫 | 開發具有臨床需求的新藥品及醫療器材 | 上櫃(6733) |
| 高端 | 利用細胞培養技術發展疫苗及生物相似藥 | 上櫃(6547) |
| 中裕新藥 | 商業模式主要為授權引進研究機構之初期之研發藥物,或者在全球尋找具特殊價值的臨床一期或二期藥物進行技術授權移轉,然後運用公司經營團隊的藥物開發經驗、專業能力,進行加值化及創新,將藥物開發至完成臨床後期或延伸應用開發新產品,之後再和合適藥廠合作共同開發、予以再授權或尋求行銷策略夥伴,以獲得相關權利金或藥物上市利益。 | 上櫃(4147) |
| 智擎生技製藥 | 專注於藥物開發,經評估及篩選在臨床前階段至早期臨床試驗階段具有發展潛力新藥,再藉由授權引進方式進行臨床開發以提升藥物價值,在臨床開發後期再授權給國際級藥廠做後續上市準備。 | 上櫃(4162) |
| 泰福生技 | 建構高表現量細胞株 | 上市(6541) |
| 藥華醫藥 | 小分子新藥、生物新藥、改良型新藥、技術平台。 | 上櫃(6446) |
| 浩鼎生技 | 生物新藥、疫苗、技術平台 | 上櫃(4174) |
表一、台灣再生醫療產業鏈(資料來源:工商時報[11])(本文自製)
第五節 精準醫療
依生醫產業發展條例草案第4條規定,是指透過基因定序或分子鑑定等之體學檢測,分析個體之生理病理特性與疾病機制及程度之關係,以提供疾病之預測、預防、診斷及治療功能,並經主管機關會同衛福部審定之創新性產品或技術。依據資誠出版的《精準醫療發展現況與趨勢》研究報告的調查結果,85%的受訪者認為未來最具潛力的市場為中國大陸、50%的認為是美國以及38%認為是東南亞、又82%的受訪者將選擇布局醫學檢測分析及診斷服務、至於47%的受訪者指精準醫療的研發經費占整體費用支出30%以上。[12]
第六節 數位醫療
依生醫產業發展條例草案第4條規定,是指以巨量資料、雲端運算、人工智慧、深度機器學習技術應用於健康醫療照護領域,且用於提升疾病之預防、診斷及治療,並經主管機關會同中央目的事業主管機關審定之創新性產品或技術。但屬人工智慧或機器學習技術之醫療器材軟體,由衛福部審定。根據市場調查公司Global Industry Analysts的調查,預計全球數位醫療市場在2026年將以18.8%的年均複合增長率成長至4569億美元;2021年上半年,美國數位醫療市場吸引了 147億美元的資金,超過2020年全年的投資金額。[13]
| 公司/機構 | 產品 | 上市櫃 |
| 筑波醫電股份有限公司 | 紅外線熱感及可見光AI自動檢篩系統、O-Ring自動手部消毒機器、智慧手寫輔助系統、生理感知器、智慧資料串流系統 | -/- |
| 研華科技 | 醫療電腦、醫療推車、醫療平板、醫療資訊終端機、醫療監視器、Intelligent Power System | 上市(2395) |
| 昊慧股份有限公司 | 醫療健康照護領域智慧化應用 | -/- |
| 玄力科技 | 資訊安全 | -/- |
| 金捷生物科技 | 遠端照護平台(母胎健康照護科技) | -/- |
| 捷而思 | 資訊安全 | -/- |
| 國眾電腦 | 智慧醫院各應用方案 | 上櫃(5410) |
| 喜海 | 通訊設備 | -/- |
| 來毅數位科技 | 醫院內部系統登入、網絡身分認證等 | -/- |
| 美維科技 | 專為醫療院所/安養機構所研發的智慧床墊系統 | -/- |
| 新鉅峰國際 | OKI雷射藥袋印表機、單張智慧藥袋、i-med健康照護 | -/- |
| 橋杭 | 智慧家居服務 | -/- |
| 凌羣電腦 | 移動護理系統、健康管理、醫院資訊管理系統 | 上市(2453) |
| 智感雲端科技 | 藍芽單導聯心電儀 | -/- |
| 巨豪實業 | 支援各式醫療場景應用的ZEBEX掃描器 | -/- |
表二、台灣數位醫療產業鏈(資料來源:數位時代[14])(本文自製)
行政院於2021年5月21日核定「六大核心戰略產業推動方案」,其中的兩核心分別涵蓋開發五項人工智慧物聯網和醫療等領域的資安解決方案以及發展精準健康產業。值得一提的是,進入數位醫療時代,應以資安應用為要。
第七節 其他策略性醫療產業
依生醫產業發展條例草案第4條規定,指經行政院指定為具策略性發展方向之生技醫藥項目,並經主管機關審定後公告者。參考修法理由,除現在新興和具策略性發展方向的生醫產品外,鑑於新型態傳染病所衍生之醫療戰略物資需求,以保自身供應之充足;另外,為了讓業者突破現有專利技術的封鎖,以推動業者積極投入該等策略性產品之研發和製造。以下舉新冠肺炎概念股為例:
| 公司/機構 | 產品 | 上市櫃 |
| 高端疫苗 | 疫苗 | 上市(6547) |
| 台康生技 | 疫苗 | 上櫃(6589) |
| 東洋藥品 | 疫苗 | 上櫃(4105) |
| 美德醫療-DR | 個人防護設備 | 上市(9103) |
| 敏成健康 | 個人防護設備 | 興櫃(4431) |
| 雃博 | 血氧機 | 上市(4106) |
| 優盛醫學科技 | 血氧機 | 上櫃(4121) |
| 太平洋醫材 | 抽痰管 | 上櫃(4126) |
| 泰博科技 | 檢測 | 上櫃(4136) |
| 瑞磁生技 | 檢測 | 上市(6598) |
| 瑞基海洋生技 | 檢測 | 上櫃(4171) |
| 寶齡富錦生技 | 檢測 | 上市(1760) |
| 亞諾法生技 | 檢測 | 上市(4133) |
| 大江生醫 | 檢測 | 上櫃(8436) |
| 普生 | 檢測 | 興櫃(4117) |
| 圓點奈米技術 | 檢測 | 興櫃(6797) |
| 長興生技 | 檢測 | 上市(1717) |
| 基亞生技 | 檢測 | 上櫃(3176) |
| 順天堂醫藥 | 清冠一號等科學中藥 | 上櫃(6535) |
表三、台灣策略性醫療產業鏈(資料來源:工商時報[15])(本文自製)
綜上所述,受到新冠疫情衝擊,衛生福利部於2021年3月31日就「COVID-19(新冠肺炎)對國內生技產業發展之影響評估,與政府因應疫情變化之施政計畫及政府針對國內相關產業的佈局與未來規劃」作出書面報告[16],乃係為因應原料藥來源短缺和原料藥價格調漲所導致藥品製劑生產成本增加,因此就需要思考重塑供應鏈的可能。例如:優化藥品查驗登記及臨床試驗等制度,前者讓國外已有之研發成功的新冠疫苗能依藥事法第48-2條為專案核准製造或輸入;後者則編列費用補助自製新冠疫苗之研發、製造,又因應緊急公共衛生情事之需,故縮短該藥品之研發時程。此外,為了滿足台灣防疫物資需求,統計自2020年至2021年3月24日的衛福部數據顯示,相關策略性醫療產品獲得許可者包括:口罩、隔離衣、額溫槍、呼吸器、鼻咽採檢機器人、小型心電圖系統以及檢驗試劑等產品。並且建立「新冠病毒篩檢及分析技術開發支援平台」和「臺灣新型嚴重特殊傳染性肺炎研究網及資料庫」,以便協助鏈結預防、診斷、治療、追蹤等策略性醫療產品的研發工作。
第二章 鼓勵發展再生醫療產業—公司成立篇
在生醫產業中,經營「研發製造新藥」或「受託開發製造生產新藥」的公司,應經主管機關審定(生醫產業發展條例草案第4條)。
首先,以經營「研發製造新藥」的公司為例,依《生技新藥公司研究與發展及人才培訓支出適用投資抵減辦法》第2條規定,符合以下各款要件的話,得向經濟部申請審定為生技新藥公司,經濟部為前述審定時,應邀財政部、衛福部、行政院農委會代表及學者專家參與;經審定為生技新藥公司者,經濟部應核發生技新藥公司審定函,並載明自核發之次日起5年內有效,屆期失其效力(同法第4條第1項):
- 從事生技新藥之研究、發展或臨床前試驗、依法規取得國內外目的事業主管機關許可進行生技新藥人體臨床試驗或田間試驗,或取得國內外目的事業主管機關發給之生技新藥上市或製造許可證明。但生技新藥之研究或發展工作全程於國外進行者,不適用之;
- 提出申請年度之上一年度或當年度之生技新藥研究與發展費用,占該公司同一年度總營業收入淨額5%以上,或占該公司同一年度實收資本額10%以上;
- 聘僱大學以上學歷生技新藥專職研究發展人員至少5人;
- 最近3年內未違反環境保護、勞工或食品安全衛生相關法律且情節重大。
其次,以經營「受託開發製造生產新藥」的公司(以下簡稱「Contract Development and Manufacturing Organization, 以下簡稱「CDMO」)為例,由於藥物開發需要龐大經費和時間,因此就有了一些在初期協助藥廠或生技公司執行各項分析、臨床準備的「委託研究機構」(CRO),以及提供製程開發、配方測試等一條龍的CDMO服務;據Frost&Sullivan和香港交易所的預估,2020年全球CDMO市場產值為555億美元,預計到2025年將以複合年成長率14%突破1000億美元;唯按目前具體劃分,仍以化學藥物為主;不過,生物藥亦在逐年攀升。[17]
第三章 鼓勵發展再生醫療產業—資金融通篇
唯鑑於生技醫藥產業具有高風險性、研發週期長、資金投入大等的產業特性,故增訂生醫產業發展條例草案第7條,係因應短期尚未能自新藥產生隱定的盈餘,即使目前已有產品上市或授權之生技新藥公司,也因持續進行其他品項研發,多數仍未有盈餘產生。因此,考慮到近年來民間游資龐大而利率創新低,為利生技醫藥產業之募資,故增訂本條提供個人股東投資生技醫藥產業金額自所得額減除之租稅優惠,以激勵個人股東投資生技醫藥產業。
相關研究指出,台灣生技業者常見的融資決策,除了現金增資和金融機構貸款外,尚有透過政府投資獎勵補助研發經費抵減、產業升級輔導方案、國發基金的投資、低利貸款、上市櫃的資金募集、由創投公司提供一定程度的募資或由第三方以轉投資的方式來挹注。[18]以下以創投浥注生技企業為例,列表台灣現階段所有之生技創投事業名稱及其資本規模:
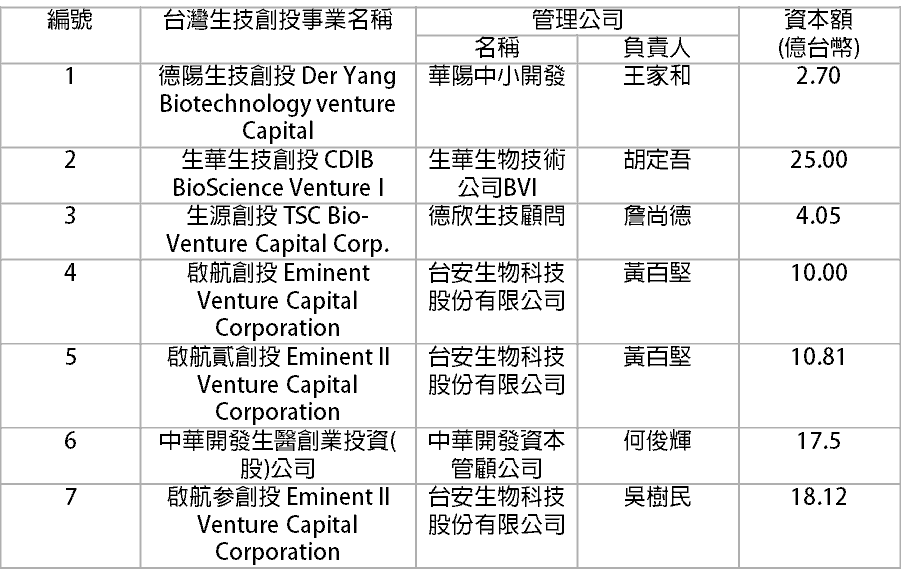
表四、台灣生技創投列表(資料來源:行政院國家發展基金管理會[19])(本文依新數據重製表格)
由上表可知,目前八家主要的投資生技創投業者之資本額為新台幣88.18億元,與過去同屬亞洲四小龍之一的韓國相比,現在的韓國(已有涵蓋共乘、生技、線上支付等領域的十家獨角獸,係指估值逾10億美元之未上市新創公司)為僅次於中國大陸和印度的亞太地區第三大新創基地。[20]另外,2021年8月5日,韓國總統文在寅在青瓦臺召開「K-全球疫苗樞紐建設願景與戰略報告大會」時指出,韓國爭取到2025年躋身全球五大疫苗生產強國之列;政府計畫在今後五年投資2.2兆韓圜(折合新台幣537億元)到疫苗、半導體、電池等國家的戰略發展產業。[21]可見,除了需要有良好的新創籌資環境外,制定有效產業政策亦是箇中關鍵。
第四章 鼓勵發展再生醫療產業—新創上市篇
台灣自2007年公布施行《生技新藥產業發展條例》,乃旨在鼓勵生技業者投入新藥開發,並引導資金及技術於生技新藥公司,基此提供其技術研發、人才培訓、法人股東等方面之租稅抵減優惠,截至2020年6月底,台灣經審定為生技新藥公司的家數共計151家,審定屬生技新藥的品項達到364項,且已有 47項取得上市許可證,對生技產業營業額的貢獻已逐年增加;據估計,截至 2019年底,生技產業營業額為新臺幣5,597億元,較2018年成長8.7%;而投資額則為新臺幣551.23億元;並且,行政院國家發展基金亦已投資15家生技公司與26家生技創投事業,該投資額為新臺幣133.5億元。[22]
觀察全球資本市場在吸引生技業者前進作首次公開募股的國家或地區中,香港交易所於2018年推行上市改革以來,香港已成為亞洲第一、全球第二的生物科技融資中心;截至2021年6月30日,已有超過50家醫療健康和生技公司在港交所提交IPO申請,當中包括19家依據《港交所上市規則與指引》18A章(生物科技公司)的準上市發行人及一家國際發行人;此外,67家已成功申請上市集資的醫療健康公司和33家未有收入的生物科技公司,籌資金額分別為2090億和870億美元。[23]值得一提的是,該33家未有收入的生技公司中,有24家的研發成本年複合成長率皆超過40%;隨著華夏恆生香港生物科技指數ETF在2021年3月正式推出,這標誌著香港資本市場生技板塊的成形。[24]
2021年台灣生技100大的資料顯示,台灣再生醫療產業擠進前百大的上市櫃公司列表如下:
| 排名 | 股票代碼 | 公司名稱 | 上市別 | 市值(億元) | 主要營業項目 |
| 2 | 6547 | 高端疫苗 | 上櫃 | 549 | 利用細胞培養技術發展疫苗及生物相似藥 |
| 16 | 4174 | 浩鼎生技 | 上櫃 | 222 | 新藥研發 |
| 17 | 6712 | 長聖生技 | 上櫃 | 217 | 幹細胞產品 |
| 25 | 6541 | 泰福-KY | 上市 | 167 | 生物相似藥及新藥研發、製造及銷售 |
| 26 | 4147 | 中裕 | 上櫃 | 161 | 新藥研發 |
| 36 | 4162 | 智擎 | 上櫃 | 95 | 新藥開發 |
| 38 | 3176 | 基亞 | 上櫃 | 90 | 生物製藥研發業務 |
| 98 | 6733 | 博晟生醫 | 上櫃 | 25 | 複合性醫材 |
表五、排名前一百名之再生醫療產業的公司(資料來源:2021台灣生技100大[25])(本文重製表格)
依上表資料顯示,2021年再生醫療產業之上市櫃公司市值總值為新台幣1526億元,約占年度生技產業新台幣1.3兆元總市值的11.74%。[26]晚近,主管機關制定《再生醫療發展法》為再生醫療之母法,法規下設再生醫療諮議會、再生醫療基金和細胞庫;母法之外,尚有《再生醫療施行管理條例》和《再生醫療製劑管理條例》,分別管理醫院再生醫療技術的推動及推動再生醫療為生技產業製劑產品。[27]三大法案目標在12月經主管機關預告,後經過60天徵詢意見後,爭取在明年1-2月彙整意見修訂、上報行政院,預計2022年會期送進立法院。[28]其目標乃係,點燃千億元之再生醫療市場。[29]
第五章 重中之中:人才運用等政策工具箱之靈活運用
為了強化台灣生技產業人才,故分別修正了生技新(醫)藥產業發展條例第5、7、8和9條,一來明定人才培訓投資抵減適用對象為專職研究發展人員;二來明定「個人股東」持股滿三年就可以在投資金額百分之五十的限度內,自第三年度起五年內減免所得額;三來讓高階專業人員和技術投資人可以取得技術股,並且若持股達兩年者,得於轉讓贈與或作為遺產分配時比較「轉讓價」或「股票取得之價格」何者孰低課稅;最後,就是放寬認股權憑證取得的股票,容許持股達兩年者,可以在轉讓贈與或作為遺產分配時比較「轉讓價」或「股票取得價格」何者孰低課稅。
此外,2019年大專院校畢業生(生命科學學門)為6,408人,占全體畢業生總數的2.13%;但如果把醫藥衛生、農業、獸醫等生技相關學門納入,就約占當年度畢業生總數的21.72%,整體生技人才約為43,700人。[30]為進一步因應台灣生技產業的人才需求,科技部制定了如下計畫:(1)臺灣-史丹福醫療器材產品設計之人才培訓計畫;(2)臺灣-柏克萊醫療器材產品設計之人才培訓計畫;(3)生醫與醫材轉譯加值人才培訓計畫;(4)科學園區高科技產業跨醫療器材產業種子培訓計畫;(5)博士創新之星計畫;(6)重點產業高階人才培訓與就業計畫。[31]近來,美國默克藥廠與台大生技中心聯合開辦了「產學未來教室」,目的為引進國際生技製藥製程技術,培育本土優秀人才,推動台灣生技醫藥產業的發展。[32]
綜合而言,不管是租稅抵免抑或人才培育,台灣生技人才尚非乏善可陳。然甚麼才是影響台灣生醫產業發展之核心要素?
首先,再生醫療是有助於人體構造或功能的重建、修復,又或是有益於人類疾病的治療與預防。因此,產品涵蓋再生醫療技術、再生醫療製劑或複合性醫療器材。值得肯定的是,主管機關為了上千億再生醫療市場的蓬勃發展,特推動《再生三法》之立法。惟從產業面向,現在已有的《生技新藥產業發展條例》(未來的生技醫藥產業發展條例草案),相關「租稅抵免」或「人才培育」等激勵措施,原條例其實已有相當規範。退一步來說,就算不另立「再生專法」,主管機關大可自藥事法第6條「凡使用於診斷、治療、減輕或預防人類疾病,或其他足以影響人類身體結構及生理機能者所稱之藥品」中「藥品」與《醫療法》中涉及「特定醫療技術」等進行法內法制化的思考。所以,著實沒有理由以「專法模式」來規範特定的商業活動,徒生思維上的負擔。
當下台灣發展生技產業之困境所在,在於市場動能不足。相較於鄰近的國家或地區(例如中國大陸、韓國),台灣不論是政府提供的優惠條件或廣大受試群體,都難以望其項背。[33]中國大陸擁有的是十四億人口的市場,而韓國則有相當於台灣人口的2.25倍。但相同的例子是,人口僅台灣一半及同為內需不足的經濟體—以色列(全球前200大企業在以色列皆設有據點),卻能在研發初期就善用全球鏈結,當進入量產階段後,快速結合猶太資本進軍美國市場,從而有利於市場量能快速達標。[34]因此, 建議政府需制定明確的政策藍圖,一來鼓勵整合島內眾多中小型生技企業,二來加深與鄰近國家或地區在資金和技術等各個層面上的合作,以利台灣生技業者進行市場拓荒。
另外,在資金挹注上,主要依靠的是行政院國家發展基金,來投資生技業者。截至2021年6月為止,國發基金直接投資生技業的總共有19家,總投資金額僅約新台幣52.49億元;而在間接投資方面,則僅有79家。[35]由此可見,不管從數量或金額來看,源自民間專業投資人(專業的機構投資人)的投資皆略顯不足。因此,需強化台灣專業投資人的基本素質,選定有潛力的獨角獸,並扶持其赴(台美)或(兩岸)資本市場雙掛牌,以連結國際資本市場,提高台灣生醫產業在國際上的能見度。
再舉以色列為例,她一向以發展生物科技而聞名,緣於該國政府採用特有的新創投資模式,以便創造極高的風險承擔與募資誘因。簡單來說,通過眾多有認證的加速器,由政府出資85 %,私人出資15%,後取得新創50%的股份,同時能獲得資金、辦公空間以及相關輔導;若新創公司虧損清算則不須賠償,但如果公司獲利,那麼政府投入資金將「以股轉債」,此時公司僅歸還本金加上若干利息即可;也就是說,相當於政府承擔了創業者一定的創業風險。[36]是故,政府應積極引導民間游資成為有潛力的加速器,繼而培養成為專業的機構投資人,後對準有發展可能性的「生技獨角獸」。
總的來說,台灣在發展生技產業的道路上,本土縱然有豐沛的研發能力,但由於市場動能不足,加上生技業者多屬中小企業,故對投資回報期長、失敗可能性高和高資本密集的生技產業而言,業者往往無法長期聚焦於特定藥物的研發,因此多採取「代工」或「一次賣斷」等方式(俗稱「CDMO模式」)來換取下一筆現金流。因此,通過吸收國際間成功的經驗,定能打造台灣成為不止在再生醫療領域,而是集全球生技產業之研發、籌資、代工、上市及製造等方面於一體的全球生技醫藥中心。
相關出版聲明
免責聲明(Disclaimer)
本期報告是針對一般性議題彙整相關資訊,並非針對特定個案表示任何專業意見,閱讀本期報告者不宜在未取得特定專業意見下,直接採用本期報告之任何資訊。「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」,包括其管理當局(合夥人)、員工及所委任之顧問,不對本期報告資訊的正確及完整與否負任何保證責任,亦不對本期報告承擔任何義務或責任。閱讀本期報告者因使用本期報告資訊所引發之任何損失、損害或任何性質之費用,「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」亦不負任何責任。
智財權聲明(Copyright Disclaimer)
本刊物是由「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」製作並擁有著作權。本刊物所有著作內容未經「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」書面同意,請勿修訂或翻印,侵害必究。
編輯團隊
眾律國際法律事務所
眾律國際專利商標事務所
眾律國際商務數位智權有限公司
范國華 主持律師/研究主持人員
吳尊傑 法務專員/協同研究人員
毛紹儒 所內專員/平面設計人員
梁祐銓 生醫領域專利工程師/諮詢顧問
媒體合作
聯絡人:吳尊傑 法務專員 電郵:kitson.wu@zoomlaw.com.tw
www.zoomlaw.online
©2021 ZoomLaw. All rights reserved.ZoomLaw refers to the ZoomLaw network and/or one or more of its affiliated firms, each of which is a separate legal entity. Please see www.zoomlaw.online for further details. This content is for general information purposes only, and should not be used as a substitute for consultation with professional advisors.
[1] 經濟日報,記者謝柏宏,「2021生技論壇/石崇良 攻三醫療產業」,2021年12月01日。https://money.udn.com/money/story/5612/5928489?from=edn_newestlist_cate_side。最後瀏覽日:2021年12月01日。
[2] 聯合報,記者沈能元,「再生醫療三法將審議 細胞治療不再是富人醫療」,2021年12月01日。https://health.udn.com/health/story/5999/5901203。最後瀏覽日:2021年12月01日。
[3] 資誠,資誠生醫透視,「全球生技製藥趨勢:再生醫學躍為醫療新主流」,頁1。https://www.pwc.tw/zh/publications/topic-bio/assets/bio-insights-2109.pdf。最後瀏覽日:2021年12月01日。
[4] 經濟部工業局,「2020生技產業白皮書」,2020年7月,頁5。https://www.biopharm.org.tw/images/2020/Biotechnology-Industry-in-Taiwan-2020.pdf。最後瀏覽日:2021年12月02日。
[5] 同上註,頁5
[6] 同上註,頁6
[7] 同上註,頁48
[8] 同上註。
[9] 衛福部食藥管理局,鄭玟君組長,「簡報:新藥審查」。https://www.fda.gov.tw/tc/includes/GetFile.ashx?id=f636694214931524687。最後瀏覽日:2021年12月10日。
[10] 產業價值鏈資訊平台,「再生醫療產業鏈簡介」,https://ic.tpex.org.tw/introduce.php?ic=C400。最後瀏覽日:2021年12月06日。
[11] 工商時報,杜蕙蓉,「再生醫療闖關 台廠盼新天堂」,2020年02月05日。https://ctee.com.tw/industrynews/consumption/211315.html。最後瀏覽日:2021年12月06日。
[12] 資誠,「精準醫療發展現況與趨勢」。https://www.pwc.tw/zh/publications/topic-bio/precision-medicine.html。最後瀏覽日:2021年12月06日。
[13] 科技產業資訊室,「COVID-19促使數位醫療投資市場爆發 2026年達4569億美元」,2021年07月12日。https://iknow.stpi.narl.org.tw/Post/Read.aspx?PostID=18023。最後瀏覽日:2021年12月06日。
[14] 數位時代,「COMPUTEX 推線上『智慧醫療館』,協助台廠進軍海外!遠距醫療、智慧照護最熱門」,2021年09月02日。https://www.bnext.com.tw/article/64857/asia-computex-cyberworld-debut。 最後瀏覽日:2021年12月07日。
[15] 工商時報,杜蕙蓉,「疫情風暴延燒!18檔新冠概念股錢來也」,2021年05月31日。https://ctee.com.tw/news/stocks/467537.html。最後瀏覽日:2021年12月07日。
[16] 衛生福利部,「COVID-19(新冠肺炎)對國內生技產業發展之影響評估,與政府因應疫情變化之施政計畫及政府針對國內相關產業的佈局與未來規劃」(書面報告),立法院第10屆第3會期社會福利及衛生環境委員會第9次全體委員會議,2021年03月31日。
[17] 數位時代,吳元熙,「【圖解】CDMO是什麼?生技界「台積電模式」,為何讓郭董大砸50億元投資?」,2021年09月30日。https://www.bnext.com.tw/article/65295/cdmo。最後瀏覽日:2021年12月08日。
[18] 黃博怡等(2016),〈政府推動創新型導向產業政策下之金融支持與策略發展模式〉,《台灣金融研訓院105年自提研究計畫》,頁50。
[19] 行政院國發基金管理會,「國發基金投資生技創投事業」,2018年01月31日。https://www.df.gov.tw/nc_13142_33269。最後瀏覽日:2021年12月08日。
[20] 工商時報,陳怡均,「韓躍亞太第3大獨角獸溫床」,2021年07月10日。https://ctee.com.tw/news/global/486618.html。最後瀏覽日:2021年12月08日。
[21] 林秀英,「【2021.08健康醫療動態】韓國未來五年將投入537億新台幣,力拼疫苗自產」,2021年08月30日。https://findit.org.tw/researchPageV2.aspx?pageId=1795。最後瀏覽日:2021年12月08日。
[22] 同前註4,頁V。
[23] 香港交易所,〈香港交易所與生物科技—開啓新章節:香港醫療健康融資生態圈蓬勃發展〉,《香港交易所與生物科技2021年7月》,頁1。https://www.hkex.com.hk/-/media/HKEX-Market/Join-Our-Markets/IPO/Biotech-Newsletter/HKEX-Biotech-Newsletter-Issue-6-CN.pdf。最後瀏覽日:2021年12月03日。
[24] 同前註4,頁2。
[25] 今周刊,呂玨陞,科技,1284期,「2021年台灣生技 100 大」,2021年07月28日。https://www.businesstoday.com.tw/article/category/183015/post/202107280058/2021%20%E5%B9%B4%E5%8F%B0%E7%81%A3%E7%94%9F%E6%8A%80%20100%20%E5%A4%A7。最後瀏覽日:2021年12月08日。
[26] 工商時報,來源:今周刊,「生技股王牌爭霸戰》合一拿下5.3億美元授權創紀錄、晶碩上半年營收25.3億元創新高…下一波潛力新星誰出頭?」,2021年07月28日。https://ctee.com.tw/bookstore/magazine/494794.html。最後瀏覽日:2021年12月08日。
[27] 聯合新聞網,來源:經濟日報,「再生醫療三法 點亮千億商機」,2021年09月21日。https://udn.com/news/story/7238/5759932。最後瀏覽日:2021年12月08日。
[28] 環球生技月刊,「石崇良再生醫療三法架構曝光 明年會期送立法院」,2021年11月23日。https://store.gbimonthly.com/Article/Detail/63697。最後瀏覽日:2021年12月08日。
[29] 同前註26。
[30] 同前註4,頁295。
[31] 同上註,頁298-301。
[32] 工商時報,鄭啟明文,「默克、台大辦產學未來教室培育生技製藥人才」,2021年08月05日。https://ctee.com.tw/industrynews/cooperation/498533.html。最後瀏覽日:2021年12月03日。
[33] KATHY HUANG,「臺灣生技產業發展趨勢系列(一):從政策、生技聚落到市場發展」,基因線上,2021年09月16日。https://geneonline.news/taiwan-biotech-industry/。最後瀏覽日:2021年12月09日。
[34] 科技魅癮,李幸宜,「鏈結矽谷與先進國家,推升產業創新動能」,2021年06月29日。https://www.charmingscitech.nat.gov.tw/post/worldview1-siliconvalley。最後瀏覽日:2021年12月10日。
[35] 同前註32。
[36] 臺北產經資訊網,「借鏡比利時、以色列、波士頓經驗,詹益鑑:台灣生技新創的發展契機來了!」,2018年10月08日。https://meet.bnext.com.tw/articles/view/43825?。最後瀏覽日:2021年12月09日。