
首卷語Preface

《眾律觀點》第二期主要收集自過去散見在本所自媒體上以及經ETtoday雲論刊登的文章,其呈現方法乃從「全球視野」及「比較視野」的角度,涵蓋了從「疫苗供給」(分配問題)到「疫苗需求」(受種者疫害損害賠償問題)的相關文章,故特由本人和法務助理吳尊傑來依前述主題適當延伸相關觀點如下:
(1)富國超量掃貨窮國買嘸疫苗新冠肺炎重塑全球公衛格局?(2)疫苗採購新加坡快速有效?!醫院採購、政府把關、專案核准(3)初探WHO全球第一個新冠疫苗無過失賠償機制(4)探討兩岸三地疫苗藥害救濟機制—以中國大陸、香港和澳門為中心(5)接種新冠疫苗後發生嚴重不良反應之救濟—以美國法為例(6)以歐盟法為例探討接種新冠疫苗後不良反應之救濟機制(7)以新加坡為例探討接種新冠疫苗後不良反應之救濟機制(8)以台灣法為中心初探完善新冠疫苗的疫害救濟之方向。
最後,吾人期待上述文章能讓台灣人民了解到在大疫之下,如何因應基於全球疫苗分布問題所衍生種種不公平現象或是作為疫苗接種親身經歷者的經驗,惟一旦發生嚴重不良反應時,相關救濟資訊之取得。
眾律國際法律事務所
范國華博士/主持律師
第一章 全球視野
第一節 富國超量掃貨窮國買嘸疫苗新冠肺炎重塑全球公衛格局?[1]
范國華/主持律師、吳尊傑/法務助理
在世界衛生組織宣布COVID-19為全球大流行的一年後,隨著疫苗的推出,全球解除隔離限制想必不是夢!然而,根據聯合國兒童基金會的數據,截至2021年2月,世界上有130個國家尚未完成接種第一劑疫苗。並且有研究發現,在較貧窮國家,約有十分之九的人沒辦法在年末前接種疫苗。
造成這種延誤的原因眾所周知,例如:疫苗稀缺和價格昂貴,而且某些疫苗需要冷鏈設備,這使得在農村地區的流通和分配變得更加困難;換言之,它們必須通過特殊的運輸和儲存等設備,以確保其在運輸或儲存的過程中,不致於受到外部溫度變化等因素的影響。
此外,低收入國家的疫苗接種還缺乏了來自於國際間合作。歐美先進國家幾乎完全專注於自己,並且很可能趕在許多國家之前,就已經為其全體人口接種疫苗。或許有些人可能會說,政府有責任在開始幫助他人之前,先解決本國的需求,即「先戴好自己的氧氣面罩後,再幫助他人」(put on your own oxygen mask first before helping others)的心態,惟此在新冠疫情全球大流行的背景下,似乎並不適用。
事實上,流行病不會在一個國家的邊界上停止,只有通過在全球範圍內徹底根除最危險形式的疾病,才能讓經濟和人民生活得以復甦。2021年1月的一項研究指出,低收入國家延遲接種疫苗可能會使富裕國家今年損失至少4.5萬億美元的收入,基於它們的經濟依賴於國際供應鏈,供應鏈中可能包括尚未接種疫苗的國家。由於人群仍未廣泛接種疫苗,因此變種病毒對其的威脅仍然存在。退步而言,變種病毒的出現可能會導致疫情在全球死灰復燃。世衛組織在敦促國際合作時肯定地說「在一場快速蔓延的大流行中,除非每個人都安全,否則沒有人是安全的。」也就是說「除非所有人都贏,否則沒有人能贏」!
富裕國家的疫苗民族主義阻礙了全球疫苗接種目標
不可避免的是,高收入和中等收入國家現在為了確保疫苗在全球範圍內的公平分配而採取的措施將決定疫情之未來發展,從長遠角度以觀,乃使疫苗成為外交談判上不可或缺的籌碼。富裕國家囤積疫苗資源的行為被視為「疫苗民族主義」,因為它出於自利,而無視全球更廣泛人口的利益。因此,疫苗或許就成為富國在外交上爭取窮國支持的籌碼。例如以疫苗來換取「窮國」在地緣政治上較親富國之既得「利益」。
儘管富裕國家僅佔世界人口的14%,但迄今為止,它們已購買了主流疫苗劑量的53%。由於不確定哪一種疫苗最終會獲批准,加拿大、英國和美國等國家聲稱有多種候選疫苗的劑量,加起來為其國家人口四到六倍的數量。
這或許緣於藥品是私有財的特性,因此衍生前述貧富不均的現象是可以預見的。簡言之,資本的多寡決定了誰可以最先獲得疫苗。在美國,聯邦政府對疫苗研究、開發以及製造的財政支持是箇中關鍵,但它附帶的條件是美國人首先獲得使用權。在疫苗獲得批准之前,富國就與疫苗開發商簽訂了雙邊預購協議,導致全球疫苗短缺和價格飆升的競購戰,結果導致窮國在競爭激烈的疫苗市場中敗下陣來。
又,疫苗民族主義和囤積性行為,亦可能會阻止跨國計劃,讓新冠疫苗全球獲取(COVAX)機制,無法實現其原初的分配目標。COVAX是與世衛組織合作創建的,旨在匯集富裕國家的資金和疫苗供應,目標是到2021年底向世界20%的人口提供疫苗。然而,該機制因缺乏資金而陷入困境。世衛總幹事譚德塞博士警告說,富裕國家的「以我為先」(me-first)的原則將使世界「處於瀕臨崩潰的邊緣」,並將為此付出代價。
截至目前,輝瑞BioNTech和Moderna疫苗已分別向富裕國家銷售96%以及100%的疫苗。阿斯利康(AstraZeneca)疫苗的前景雖看似良好,該公司宣布其64%的疫苗供應將流向較貧窮的國家。惟近來由於AZ疫苗頻繁出現接種後發生血栓等不良反應,而被各國停止施打。另外,疫苗民族主義的後果,乃迫使中低收入國家考慮使用中國大陸製造的科興、國藥以及俄羅斯Sputnik V等的新冠疫苗。
雖然如此,但像擁有龐大人口的中、印兩國,基於本身也有大量人口需接種疫苗。尤其是在中國最近的一次疫情中,迫使其人口接種疫苗的時程變得更加緊迫,故推遲了向其他國家承諾的疫苗劑量的供應。另外,2021年3月下旬,由於印度國內疫情持續延燒,該國暫停疫苗的出口,因為僅提供印度約2億弱勢人口接種疫苗,就需要大量疫苗。
儘管存在這些挑戰,但全球公共衛生的格局確實發生了變化,即降低中、低收入國家對歐美地區的依賴,取而代之的是依賴於鄰國或地區大國,並向同樣富裕的國家求助。不管是中國大陸提供的科興、國藥、康希諾等疫苗,抑或是由俄羅斯、古巴等地生產的疫苗,前述皆為少數將低收入國家的需求放在首位的疫苗生產商之一。
最後,當西方的疫苗生產商與富國簽訂雙邊協議時,中、印、俄等國正考慮如何將自己的「疫苗供給」與「疫病需求」國家結合起來。前述國家也非完全出於「公益考量」;相反,她們意識到西方國家未能挺身應對疫苗供不應求的危機,於是成為他們確立在全球公共衛生領域的領導者的絕佳機會。更甚者,就是讓中等收入國家認識到疫情的終結,乃緣於國際合作,而非孤立主義。換言之,即取決於雙贏戰略之實施!
第二節 疫苗採購新加坡快速有效?!醫院採購、政府把關、專案核准[2]
范國華/主持律師、吳尊傑/法務助理
近來,依據新加坡衛生部相關公告顯示,若干種被世界衛生組織核准並列入「緊急用途清單」(emergency-use listing)的新冠疫苗,乃得以在所謂特殊通道(Pandemic Special Access Route,下稱「PSAR」) 下被緊急授權使用。[3]至於歐盟的疫苗策略,歐盟委員會為因應新冠疫情,故先後於2020年12月21日、2021年1月6日、29日和3月11日,授予BioNTech疫苗、Moderna疫苗、AstraZeneca疫苗以及Johnson & Johnson疫苗之有條件行銷權。[4]本文以下將比較新加坡「合資格醫療機構」採購模式與歐盟委員會授權境內外「疫苗開發商」申請使用、行銷於域內時所遵循之標準及程序,希望可以提供臺灣作參考之用。
首先,新加坡的緊急授權指南係依據《健康產品(醫療產品)條例》(Health Product (Therapeutic Products) Regulations,下稱「健康產品條例」)第60A(4)及(5)(b)之臨時授權(The interim authorisation)條款下「緊急醫療產品」供應之特殊通道,即「PSAR」。前述臨時授權機制使監管機構得以靈活應對可能對公眾構成嚴重威脅之緊急情況,特別在「大流行」(Pandemic)的情況下。唯鑑於緊迫的公共衛生需求,新加坡衛生科學局(HAS)將優先審查新型療法和疫苗,以促進及時獲取,同時對其質量、安全性以及有效性評估之科學嚴謹性進行擔保。此外,PSAR規定新加坡政府在「大流行」期間指導此類緊急醫療產品之供應,並且需考慮以下幾點:(1)有合理的證據表明,在緊急情況下得以治療或預防對公眾構成嚴重威脅之疾病,其潛在收益大於風險;以及(2)正在生成中的質量、安全性以及有效性數據,以確保其得以依據《健康產品法》第15條及第22條的規定從臨時授權過渡至產品之最終註冊。[5]本條例係自2016年11月1日起開始實施。
具體而言,當合資格醫療機構或公司之持牌人欲就緊急醫療用品提出臨時授權之申請時,申請人必須確保其滿足以下先決條件:[6](1)申請人是受新加坡政府指示為政府或代表政府供貨之合資格醫療機構或公司;和(2)該醫療用品已被新加坡政府評估為滿足健康產品條例第2(a)條規定之一項或多項條件。惟在提出申請之前,合資格醫療機構或公司須進入申請前的諮詢程序,也就是需先通知HSA,以便進行諮詢程序以討論相關數據提交計劃。然而,HSA亦得以該請求不具理由而為不予答覆之處分。當局因應臨時授權之急迫性,故就申請所需的證據等級提供了靈活性,即允許以滾動方式提交數據(rolling basis)。包括但不限於提供得用於啟動審查程序與文件資訊之初始數據,以及後續數據提交之順序和時間表。
而在歐盟,[7]歐洲藥品管理局(下稱「管理局」)甚至在疫苗開發公司請求批准疫苗之前,就開始查看相關臨床數據。一般而言,與所有藥物一樣,疫苗首先在實驗室內進行測試。爾後,需在幾輪臨床試驗中針對人類志願者進行測試。臨床試驗有助於確認疫苗的運作機理,並確保其益處超過任何潛在的副作用或風險。一旦有了足夠的研究及臨床數據,疫苗開發公司就可以向管理局申請授權,將疫苗投放市場。管理局評估所有數據並對疫苗進行獨立和徹底的科學評估,以此作為歐盟委員會是否授予其在歐盟之行銷權的基礎。不過,在新冠肺炎大流行期間,就例外允許管理局得授予藥品或疫苗之於有條件的行銷權。在這種情況下,生產商除了承諾依照規定的時間表提供額外的資訊,惟尚需接受歐盟固有藥物監測系統就獲得有條件上市授權的疫苗就安全性以及有效性之嚴格監控。並且採取得以快速收集和評估新資訊的特殊措施。舉新冠疫苗為例,基於接種人數眾多,故除了須每月繳交安全報告外,管理局另需設置額外的大規模安全監測機制。
不過,與新加坡不同的是,歐盟的「有條件授權」及「採購」乃是統一由歐盟委員會處理,爾後再由各成員國之主管機關接手制訂接種和配送作業流程。惟單從申請授權使用不同廠牌的新冠疫苗的當事人(新加坡乃合資格醫療機構之持牌人,而歐盟則為疫苗開發商)而言,皆需提供持續的科學研究數據以證明該疫苗的潛在益處大於其已知風險或副作用,基此合乎兩地主管機關的授權標準以及程序後,方得為臨時授權或有條件授權之使用。以下表比較之:
| 要件 國別 | 新加坡《健康產品條例》第60A條—緊急醫療產品的製造、進口及供應之例外規定 | 歐洲聯盟則透過疫苗透明度及授權機制 |
| 申請人 | 第5(a)(1)條規定申請人得提供、維護或確保該提供、維護處理和儲存醫療產品所需之人員、場所、設備及設施,以防止對醫療產品有所有權、佔有或控制權之申請人在使用期間變質。 申請人必須滿足以下要求之一: 5(b)(1)(i)規定之代表私人醫院或診所之醫療保健機構持牌人得為「申請人」,乃由私人醫院或診所執業之合資格醫生所開具的有效處方來進口,以便供其病人使用。 5(b)(1) (ii)旨在僅用於科學教育或研究和開發目的,或用於非臨床目的; 5(b)(1) (iii) 僅為出口目的而進口; 5(b)(1) (iv) 旨在提供在船上使用,並且醫療產品是根據《商船(醫療用品)規例》(第 179 章)要求在船上攜帶的藥品,商船2014 年航運(海事勞工公約)(藥品和醫療設備)條例(GN No. S 181/2014)或任何其他成文法,關於船上人員的待遇; 5(b)(1) (v) 旨在提供在飛機上使用,並且醫療產品構成《空中航行令》(第6章)或任何其他成文法規定的醫療用品的一部分,用於治療登機乘客; 5(b)(1) (vi)被醫療產品的註冊人授權進口;或者 5(b)(1) (vii)在所有方面與註冊醫療產品相同,而註冊人並未授權申請人進口該註冊醫療產品;及 (c) 如果醫療產品是按照 (b)(i)、(vi)項進口的,申請人能夠遵守管理局網站上列出的管理局關於進口商良好分銷規範的指導說明中的要求) 和 (vii)。 (2) 除第 (1) 款的要求外,擬根據第 (1)(b)(vii) 款進口醫療產品的申請人必須為每批進口的此類醫療產品獲得管理局的事先批准。 (3) 根據第(1)款申請管理局批准的申請必須以管理局網站上指明的格式和方式提出。 | 歐盟並不允許成員國內合資格的個人或機構申請進口疫苗,而是由歐盟委員會統一為安全、有效的疫苗 授權域內使用暨與疫苗開發公司議定採購契約,再由成員國之主管機關為以下的作業: 除了有權決定接種新冠疫苗的順序外,更可以通過國家疫苗接種計劃來分配疫苗。值得一提的是,歐盟藥品管理局並不參與疫苗的分配及流通。 |
| 行為類型 | 例外允許為政府或代表政府製造、進口、批發以及供應特定的緊急醫療產品。 | 經歐盟委員會批准的新冠疫苗:[8]獲授權上市之申請人就需要確保是否具有快速且大規模生產及分銷的能力。換言之,多數申請人為爭取時間,故在獲得上市授權之前,就已經開始其提高產能及生產程序之活動。 |
| 定義 | 須先符合「民防緊急情況」的規定,係指根據《民防法》(第42章)第102(1)條宣布的民防緊急情況。後續方可申請進口「緊急醫療產品」,乃指部長為本條例的目的指定為緊急醫療產品之相關醫療產品。一般民防緊急情況,是在「傳染病」大流行期間,係指具有《傳染病法》(第137 章)第2節賦予的含義。 | 歐盟並沒有就「緊急醫療產品」進行定義。僅定義所謂「新冠疫苗」,乃是通過觸發免疫系統反應來預防由新型冠狀病毒(SARS-CoV-2)引起的疾病的藥物。[9] |
| 核准條件 | 治療因民防緊急情況導致之任何醫療狀況;防止傳染病的傳播或可能的爆發;或治療傳染病或與傳染病有關的任何醫療狀況,如果該醫療狀況或傳染病可能嚴重或危及生命。 | 管理局評估所有數據並對疫苗進行獨立和徹底的科學評估,以此作為歐盟委員會是否授予其在歐盟境內行銷權的基礎。 |
| 裁量基準 | 初步科學證據表明醫療產品係具有以下潛力: 治療因民防緊急情況導致的醫療狀況;防止傳染病的傳播或可能爆發;或治療傳染病或與傳染病有關的任何醫療狀況,視情況而定;和對使用醫療產品的人來說,持續的科學證據表明醫療產品的潛在益處超過其已知風險。 | 疫苗生產商除了承諾依照規定的時間表提供額外的資訊外,尚需接受歐盟固有藥物監測系統就獲得有條件上市授權的疫苗之安全性及有效性進行嚴格監控。並採取得以快速收集及評估新資訊之特殊措施。以新冠疫苗為例,基於接種人數眾多,故除了需要每月繳交安全報告外,管理局另需設置額外的大規模安全監測機制。 |
[8] See, How are vaccines being rolled out in the EU?. https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/vaccines-covid-19/covid-19-vaccines-key-facts#how-are-vaccines-being-rolled-out-in-the-eu?-section. Last visited 9 June 2021.
[9] See EU, COVID-19 vaccines: key facts. https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/vaccines-covid-19/covid-19-vaccines-key-facts. Last visited 9 June 2021.
最後,觀看臺灣《藥事法》第48條之2,乃規定中央衛生主管機關得以「專案核准」特定藥物之製造或輸入,不受第39條及第40條之限制。基此,似乎是偏向歐盟式「中央統籌機制」。惟觀之於現階段臺灣本土疫情,其日增確診病例截止2021年6月10日,已連續3週以3位數字成長,累計確診為11,968例;更為嚴竣的是,死亡人數現已累積到333例!因此,主管機關有必要改採新加坡的「合資格醫療機構採購,並由政府把關」之模式,來作出「臨時性」「專案核准」之決定,並在成立專家審查小組的前提上,方便後續檢討、修正「專案核准」後疫苗之採購及施打期程。
第二章 比較視野
第一節 初探WHO全球第一個新冠疫苗無過失賠償機制
范國華/主持律師、吳尊傑/法務助理
今年的年初,世界衛生組織(World Health Organization, WHO)同意通過全球首個疫苗無過失賠償計劃(No-fault compensation programme for COVID-19 vaccines,下稱「賠償計劃」),以期解決因通過新型冠状病毒疫苗全球實施計劃(COVID-19 Vaccines Global Access, COVAX)取得新冠疫苗而導致92個較貧窮國家的人們出現嚴重副作用的損害賠償請求權的問題,力求提供一次性無過失損害賠償;此外,賠償計劃旨在顯著減少人民訴諸有著冗長且成本高昂的法院審判過程。[10]作為全球首個疫苗傷害賠償機制,賠償計劃將為具有全球疫苗免疫聯盟新冠疫苗預先市場承諾(the COVID-19 Vaccines Advance Market Commitment, AMC)資格的國家和經濟體中,提供符合條件者一個快速、公平、健全和透明的流程,以利在2022年6月30日前對與受COVAX分配的疫苗有關的罕見但嚴重的不良事件進行賠償。[11]
唯首先,要成為COVAX全球受分配之疫苗,需被WHO列入「緊急使用清單」(Emergency Use Listing, EUL)中的疫苗。所謂「緊急使用清單」,緣於2017年5月在瑞士舉行的關於世衛組織改進監管準備以應對突發公共衛生事件的各種選擇的非正式磋商會議中得出結論,世衛組織EUAL程序(Emergency Use Assessment and Listing, EUAL)的某些方面需要重新考慮和修訂,會後得出以下共識:(1)該流程應重新定義為「緊急使用清單」(EUL)程序;(2)修訂後的程序應主要使用於國際關注的突發公共衛生事件(Public Health Emergency of International Concern, PHEIC)期間,儘管世衛總幹事得授權在不符合PHEIC標準的其他突發公共衛生事件中使用此程序,惟仍需確定是否符合公共衛生之最佳利益;(3)世衛組織應確保在EUL框架下使用未經授權的產品,須是基於預先確定的理由及標準;(4)國家監管機構 (National Regulatory Authorities, NRA) 的作用及對其評估的依賴程度應明確,至於潛在受影響國家的NRA則應參與突發公共衛生事件期間的EUL程序;最後(5)EUL尚應包括緊急情況前活動的計劃,以便在宣布緊急情況後迅速作出上市決定;是故如此EUL程序取代了EUAL程序。[12]
下表是EUL程序的流程圖:[14]
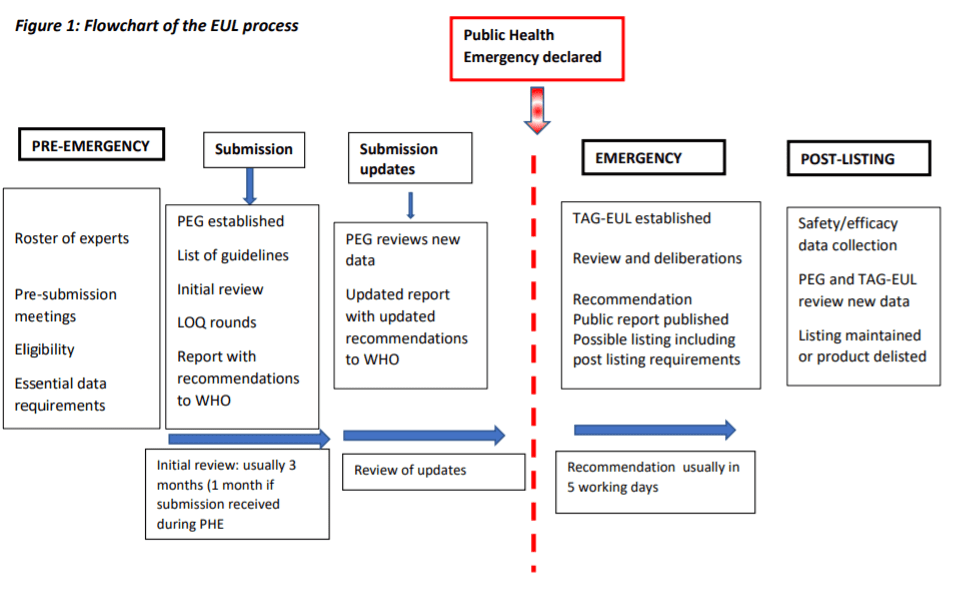
(資料來源:世衛緊急使用清單程序)
雖然目前僅有24個國家或地區擁有常規免疫接種的無過失疫苗損害賠償系統,但在世界衛生組織晚近同意承保一項針對嚴重副作用而請求無過失損害賠償計劃中,一來為受COVAX分配疫苗的92個較貧窮的國家,提供一次性紛爭解決機制,減省訴諸法院之應訴負擔;二來則為疫苗生產商提供伴隨補償的疫苗損害賠償計劃,通過設計來降低生產商之財務風險。然前述也可以被視為降低了生產商對其疫苗安全性之責任;但另一方面,生產商亦需要仔細傳達關於疫苗製作的基本原理,藉以消除那一群乃特別是在已經對疫苗的安全性和有效性起懷疑態度的特定人群中。[15]
最後,若有民眾是通過接種6月30日前受COVAX機制分配之疫苗,並在後續產生嚴重不良事件導致永久性損害或死亡者,就有獲得該賠償計劃授予安全、終局且一次性無過失之損害賠償救濟途徑。因此,相關人可以前去「COVAX No-Fault Compensation Program」的入口網站(https://covaxclaims.com/),以便及時獲得有用的救濟資訊。
第二節 探討兩岸三地疫苗藥害救濟機制—以中國大陸、香港和澳門為中心
范國華/主持律師、吳尊傑/法務助理
本文將會就中國大陸、香港和澳門的新冠疫苗接種後嚴重不良反應的救濟機制進行討論、說明。首先,目前供應澳門的兩款新冠疫苗主要來自於北京國藥的滅活疫苗以及輝瑞BioNtech的疫苗;截至2021年7月16日為止,累計1,914例不良事件通報,包括6例嚴重不良事件以及1,908例輕微不良事件。[16]至於香港,目前主要施打的疫苗為採用滅活技術的科興疫苗和採用RNA技術的復必泰疫苗;同樣地,截至2021年06月30日為止,香港衛生署共接獲4,010例異常事件報告(平均每接種十萬劑就有107.5例(0.11%));其中,接種科興和復必泰疫苗後出現不良反應的報告分別有2052例及1958例。[17]而觀中國大陸,統計自2020年12月15起至2021至11月23日,全國已接種疫苗者有244942.7萬劑次[18],報告預防接種不良反應31434例,報告發生率為11. 86/10萬劑次,其中嚴重異常反應發生率為0.07/10萬劑次,發生概率在低於萬分之一的範圍以內。[19]以下將依次進行討論。
先說澳門,2021年02月26日,由特區行政長官依據基本法第50條和《防疫接種制度》第四條第一項批准的《澳門特別行政區防疫接種特別計劃》,公布新冠疫苗接種計劃包括「滅活疫苗」(即「國藥疫苗」)和「信使核糖核酸疫苗」(即「復必泰疫苗」)的兩款疫苗。[20]前述第四條第一款乃指於特定時期內,有必要在澳門接種的計劃外疫苗的種類、適用人群和接種程序,由行政長官以批示核准,並公佈於《澳門特別行政區公報》。但如果接種者發生因接種引起嚴重不良反應,則醫務人員應自知悉相關情事起七十二小時內向衛生局通報。[21]話說一旦導致嚴重事故者,按澳門政府目前已選定「忠誠澳門保險公司」作為「向衛生局提供接種新冠病毒疫苗不良反應/副作用保障」的公司,由政府為年齡介於十六至八十五歲接種者購買該以一年為投保期以及九十天保障期的團體保險,保額最高為一百萬澳門元。[22]惟理賠的條件是該不良事件究自疫苗導致、焦慮等的心理反應所造成、偶合事件、疫苗生產或使用程序錯誤等不確定性因素所引起,皆需經過專家分析來作出基於世衛的因果關係評估流程的判斷。[23]
其次,香港政府考慮到當前公共衞生緊急狀態,又為了引入符合安全、效能及質素要求的新冠疫苗作緊急使用,故於2020年12月23日訂立《預防及控制疾病(使用疫苗)規例》(第599K章)(下稱「規例」),以利提供法律框架。目前,「規例」授權食物及衞生局局長,根據一款新冠疫苗的客觀醫學數據(包括第三期臨床研究數據),參考一個由行政長官委任成立的「2019年冠狀病毒獨立顧問專家委員會」的專業意見,及參照一個本港以外藥物監管機構核准使用(包括緊急使用),經評估在科學上符合安全性、有效性之要求,並同時符合品質保證的背書,得認可目前兩款新冠疫苗(即復必泰和科興疫苗),批准前述疫苗在香港基於緊急情況下作指明用途,包括由政府推行之疫苗接種計劃。[24]不過,對於因接種疫苗而產生副作用的人而言,所有提報個案皆需由醫護人員經衞生署的藥物安全監察系統向衞生署呈報,專家委員會在收到後隨即按世衞的因果關係評估算法流程進行潛在因果關係的判斷。後續則在2019冠狀病毒病疫苗安全監測計劃下,由醫管局和衞生署建立機制,將一些不符合呈報為異常事件的死亡個案紀錄提供給香港大學進行監測及分析,而有關研究結果亦會定期向專家委員會匯報。假如香港大學發現有不尋常的情況,會盡快通知衞生署及交予專家委員會作出跟進。[25]至於若符合如下條件者:(1)該嚴重異常事件已得到註冊醫生證明;以及(2)新冠疫苗臨床事件評估專家委員會的評估結果未能排除該事件與接種政府疫苗接種計劃下提供的新冠疫苗無關。則由政府委任的第三方行政管理人—安盛金融有限公司(下稱「AXA 安盛」)設立之「異常事件保障基金」,接手審查申請人之相關證明文件,以便提供及時的財政援助。[26]
最後,若談及中國大陸的救濟機制,乃依據《藥品管理法》第6條規定之藥品上市許可持有人,需依法對藥品研製、生產、經營、使用全過程中藥品的安全性、有效性和質量可控性負責。在一般情況下,若發現有疑似不良反應者,則依同法第81條規定應及時向藥品監督管理部門和衛生健康主管部門報告;具體辦法由國務院藥品監督管理部門會同國務院衛生健康主管部門制定。惟在新冠大流行期間,依據《傳染病防治法》第15條第1項規定「國家實行有計劃的預防接種制度。國務院衛生行政部門和省、自治區、直轄市人民政府衛生行政部門,根據傳染病預防、控制的需要,制定傳染病預防接種規劃並組織實施。」相關疫苗(例如:國藥和科興),由國務院於2020年7月22日批准之《新冠病毒疫苗緊急使用(試用)方案》(下稱「緊急使用試用方案」),以啟動疫苗的緊急使用。[27]而為了落實疫苗緊急上市許可持有人的責任,且保障消費者的合法權益,中國大陸隨即以徵求意見稿的形成公布《疫苗責任強制保險管理辦法》,以因接種疫苗的質量問題導致受種者之損害,依法應以負賠償責任為保險標的之保險。[28]但有下列情形之一者:(1)預防接種異常反應、因疫苗本身特性引起的接種後一般反應、受種者在接種時正處於某種疾病的潛伏期或者前驅期,接種後偶合發病、受種者有疫苗說明書規定的接種禁忌,在接種前受種者或者其監護人未如實提供受種者的健康狀況和接種禁忌等情況,接種後受種者原有疾病急性復發或者病情加重、因心理因素發生的個體或者群體的心因性反應,以及其他不屬於疫苗品質問題的情形;(2)因疫苗上市許可持有人或者其委託儲存運輸的單位以外的其他協力廠商原因導致疫苗出現品質問題的;(3)因疫苗上市許可持有人故意實施違法行為,導致疫苗出現品質問題的;(4)預防接種事故;則保險公司不予賠償。[29]總之,中國大陸是以疫苗上市許可持有人在許可後、銷售前,應與保險公司依法訂立保險契約,投保疫苗責任強制保險。[30]以中國大陸保險行業協會(下稱「保險業協會」)晚近向行內發佈《新冠病毒疫苗預防接種異常反應補償保險示範條款(試行版)》(下稱「示範條款」)為例,乃規定以下三種保險責任:(1)經有關衛生主管部門、藥品監督管理部門或其指定的相關部門出具預防接種異常反應診斷結論或鑒定書,保險人須依約定作出賠償;(2)保險事故發生後產生的鑒定費用、屍檢費用、傷殘等級評定費用等其他必要的、合理的費用,保險人按照本保險契約約定負責賠償;和(3)保險事故發生後,因保險事故而被提起仲裁或者訴訟的被保險人,對應由被保險人支付的仲裁或訴訟費用以及事先經保險人書面同意支付的其他必要及合理的法律費用,保險人按照本保險契約約定負責賠償。[31]
綜上所述,舉凡兩岸三地乃是採取保險(中國大陸、澳門)以及保障基金(香港)的方式,以便對依疫害因果關係判定之受種人作出賠償。惟不同的是,有鑑於中國大陸作為疫苗生產大國,則需以「強制生產商投保」的方式來免除受種者對疫苗生產商之請求權基礎。
第三節 接種新冠疫苗後發生嚴重不良反應之救濟—以美國法為例
范國華/主持律師、吳尊傑/法務助理
自新冠大疫以來,各國皆卯足全力來研製相關的疫苗。唯基於疫苗乃有助於阻隔許多致命傳染病之傳播,從而有利於公眾健康的福祉。故隨著晚近各種新冠疫苗的問世,作為過去新冠疫情嚴重的國家之一—美國,如今約1.6億人(相當於美國總人口的一半)接種了疫苗。[32]惟不幸的是,部分接種新冠疫苗的人產生了有害的副作用。[33] 舉例如:嬌生公司最近開發的新冠疫苗(J&J Vaccine)被美國食品及藥物管理局(U.S. Food & Drug Administration, FDC)以及美國疾病管制與預防中心(Centers for Disease Control and Prevention, CDC)暫停使用於短期內作為疾病控制與預防之藥物,以便對少數接種該種疫苗的人的血凝塊報告病例進行研究。[34]有鑑於此,部分接種該疫苗後出現副作用的人,就希望提起損害賠償請求權之訴。不過,關於疫苗損害賠償請求權之處理方式實與大多數醫療侵權損害賠償不同。本文以下將以美國法為例,就當事人如何主張疫苗損害賠償請求權進行討論。
首先,美國「國家疫苗損害補償計劃」 (the National Vaccine Injury Compensation Program,VICP) 得以向因接種VICP所涵蓋之疫苗而招致損害的請願人提供經濟補償。即使是在沒有作出此類調查結果的情況下,請願人亦得以通過和解來獲得補償。本文將說明其運作機制:[35]
VICP是如何運作的?
國家疫苗損害賠償計劃是作為傳統法律體系中無法解決疫苗損害補償申請的基於無過失責任之替代方案。它創建於1980年代,乃針對緣自於疫苗公司及醫療保健提供者之訴訟威脅,立法者為了避免導致疫苗短缺致使降低美國疫苗接種率,是故為了平衡各方的利益,就有了該項計劃的通過。計劃允許處於任何年齡之個人,如果接種了承保疫苗並認為自己因此受傷,都可以提交請願書。至於父母、法定監護人以及法定代表人,亦得代表兒童、殘疾人及已故的個人提交申請。
具體流程如何?
- 首先,個人向美國聯邦索賠法院(United States Court of Federal Claims;Fed. Cl. or C.F.C.)提交請願書;
- 其次,由美國衛生與公共服務部(The U.S. Department of Health and Human Services, HHS)的醫務人員審查請願書,確定它是否符合醫療補償的標準,爾後提出初步建議(preliminary recommendation);
- 其三,由美國司法部制作一份報告,報告包括相關醫療建議以及法律分析,並將其提交於法院;
- 其四,報告提交給法院指定的特別主管(court-appointed special master),乃指通常在舉行雙方都可以提供證據的聽證會之後,作出是否補償請願人的決定。如果當事人獲得補償,則由特別主管確定補償之金額和類型;
- 其五,法院命令美國衛生與公共服務部給予補償。即使申請被駁回,惟若滿足某些要求,法院亦得命令該部門支付律師費以及相關費用;
- 最後,當事人可以對特別主管之決定提出上訴,或拒絕法院決定(或在特定期限內撤回其申請)的請願人得以向民事法庭提起針對疫苗公司或者負責接種疫苗的醫療保健提供者的損害補償之訴。
《PREP法案》與限制因醫療對策而生之責任[36]
然而,為了鼓勵在突發公共衛生事件期間迅速制定和部署醫療對策(countermeasures),《公共準備和應急準備法案》(the Public Readiness and Emergency Preparedness Act,下稱「PREP法案」)授權HHS限制與醫療對策有關損失(例如:診斷、治療和疫苗等)之法律責任。在2020年2月4日生效的HHS聲明中,HHS部長援引了PREP法案,並宣布2019年新型冠狀病毒為突發公共衛生事件,需要就涵蓋的對策提供責任保護。根據HHS聲明及其修正案,涉及的人員通常免於因與管理或使用針對新冠病毒的涵蓋對策有關的損失而承擔法律責任,簡單來說他們不能在法庭上因金錢損害而被起訴。惟PREP法案下豁免醫療對策的責任之唯一例外,乃需因「故意不當行為」(willful misconduct)而導致死亡或嚴重身體損害。因此,受涵蓋對策直接導致死亡或重傷者,就有資格通過「損害補償對策計畫」(Countermeasures Injury Compensation Program, CICP)向該對策之主管機關請求補償損失。值得一提,與CICP不同的是,VICP為在美國常規接種的大多數疫苗造成的損害提供補償,例如:兒童(包括MMR、脊髓灰質炎、甲型肝炎)和非大流行性季節性流感的疫苗。相比之下,CICP 僅適用於PREP法案宣布的突發公共衛生事件所涵蓋的對策,例如:針對新冠病毒、大流行性流感(例如:2009 H1N1「豬流感」)以及伊波拉病毒發布的對策。又,VICP 的資金來自對CDC推薦用於兒童或孕婦常規接種的許可疫苗的消費稅。故一般而言,CICP的補償會比VICP更為有限。即無法通過CICP獲得律師費以及請求精神上損害賠償,並且法規也不允許對HHS的CICP補償決定進行司法審查。
法院將PREP法案的責任豁免定性為「全面性」的,乃適用於州和聯邦法律所規定的所有類型的合法請求權。舉例如依照州侵權法,若因他人的故意或過失的作為或不作為而招致傷害者,則通常可以起訴該人以獲取金錢賠償。因此,在醫療服務的環境中,如果醫療服務提供者因過失管理藥物或設備而對患者造成可預見的傷害時,那麼受傷者得依據州侵權法起訴該醫療服務提供者,並請求賠償。
在某些情況下,諸如PREP法案之類的聯邦法律可能優先於州侵權法以及其他州和聯邦的法律。基於聯邦先占立法取代了州法律,以改變通常的責任規則或使某些個人免於承擔責任。在PREP法案中,國會在突發公共衛生事件的背景下作出判斷,即免除某些人和實體之責任,以確保其有效地制定、部署和管理可能用於挽救生命之對策。
總之,因接種新冠疫苗後出現的嚴重不良反應,就當事人之損害補償救濟而言,不管是VICP或CICP,皆可以提供當事人相關便捷和有效的救濟途徑。反之,對服務提供者或生產商而言,則除非是出於「故意且不當的行為」;否則就可以在PREP法案下獲得豁免責任的保護。
第四節 以歐盟法為例探討接種新冠疫苗後不良反應之救濟機制
范國華/主持律師、吳尊傑/法務助理
所謂歐盟的疫苗傷害補償計劃[37](Vaccine injury compensation programmes, VICPs),乃是歐盟各成員國為了補償遭受嚴重疫苗傷害者所建立的「無過失計劃」(下稱「該計劃」)。誠如專門術語「無過失」所指的是,VICP不要求受害方或其法律代表在賠償之前證明疫苗供應商、醫療保健系統或製造商的疏忽或過失,而是尋求不通過訴訟來獲得疫苗相關損害賠償的必要性,因為訴訟程序冗長且難以證明顯著的過失。在無過失的責任原則下,政府補償因正確製造的疫苗而受到傷害的個人,目的是消除個人對製造商使用法律或其他程序的需要。
唯在全球範圍內,有25個司法管轄區擁有VICP制度,其中的16個是歐洲國家,諸如:奧地利、丹麥、芬蘭、法國、德國、匈牙利、冰島、意大利、盧森堡、挪威、俄羅斯(非歐盟成員國)、拉脫維亞、斯洛文尼亞、瑞典、瑞士以及英國(前歐盟成員國)。在如今新冠病毒大流行的背景下,圍繞VICP的爭論可以說變得越來越重要,因為計劃允許向從已批准上市的新冠病毒疫苗製造商處購買疫苗的一方提供法定補償機制,也就是說購買協議的買方不能要求製造商賠償因疫苗而有之損失。
歐盟早期與人體醫藥品有關之立法
在2001年11月6日,歐洲議會和理事會修訂關於針對人體藥品相關(medicinal products for human use)的歐盟共同體法律指令:2001/83/EC(下稱「該指令」),[38]乃鞏固歐盟早期與人體醫藥產品相關的立法,並且仍然作為歐盟主要立法例而存在。該指令與其他歐盟指令被轉化為歐盟成員國的國家法律,並由其國家主管機關、各國法院以及歐洲法院(European Court of Justice)來實施、應用、解釋以及執行。
與美國《公共準備和應急預備法》(Public Readiness and Emergency Preparedness Act, 下稱「PREP法案」)法案相似,該指令廣泛適用於所有「醫藥產品」之中。然相較之下,提供予參與新冠病毒醫藥產品供應者的豁免範圍卻比PREP法案更窄。該指令第5(3)條要求成員國制定法律,以保護獲上市授權之藥品所有人、製造商以及醫療保健專業人員等,免於因使用未經授權的醫藥產品而產生的任何後果的民事或行政責任;若歐盟成員國的主管部門要求或推薦此類使用以應對新冠病毒大流行,則授權藥品的標籤外使用。此類保護的範圍得因成員國而異,具體取決於實施該指令第5(3)條的各國法律所用文義。
惟除此之外,該供人體使用的醫藥產品之製造商尚可提出所謂「開發風險抗辯」,縱然該指令第5(4)條規定第5(3)條有對製造商所為相關責任限制,但亦不影響歐盟指令第85/374/EEC(下稱為「瑕疵產品責任指令」)對其的適用問題。即若醫藥品不能「基於所有情況提供人們對疫苗安全性之有權期待,則該醫藥品將被認為是有缺陷的。」例如,這有可能適用於藥品生產中出現的質量問題。換言之,這就是瑕疵產品責任指令下諸多抗辯之一—「開發風險抗辯」(development risks defense),意即若生產者能夠證明「就當時科學與技術知識之狀態而言,即當他將產品投入流通時,並不能發現缺陷之存在」(the state of scientific and technical knowledge at the time when he put the product into circulation was not such as to enable the existence of the defect to be discovered),則得執此為免責之事由。[39]
儘管歐盟成員國間一直抵制針對醫藥產品製造商所有的豁免權,包括在大流行中開發的醫藥產品,惟前述瑕疵產品責任指令亦可在一定程度上減輕責任認定的風險。因此,當評估產品是否存在「瑕疵」(defect)時,需考慮的情況包括其是否屬於在大流行下加速開發的(包括但不限於存在有條件上市授權等的事實);基此,相關「開發風險抗辯」就很可能會被適用。然而,由於相關指令下的抗辯依然不能讓製造商免於訴訟的威脅。即此之故,就有「該計劃」存在之意義,但肯否意見者俱在。
肯定該計劃者認為:(1)代表政府承擔道德責任;(2)VICP 保護疫苗製造商免受代價高昂的訴訟威脅;(3)VICP 有助於確保疫苗的供應;(4)VICP 鼓勵公眾對疫苗的信心。相反,否定論者則認為:(1)VICP 損害了公眾對疫苗的信心;(2)VICP對財政來說是昂貴的;(3)疫苗和傷害之間的因果關係難以確定;(4)VICP 使製造商在其產品造成危害的情況下不受懲罰。[40]
代結論:關於補償基金之資金來源
回歸正傳,對於因接種疫苗而招致之損失,由於歐盟現階段尚未設置「泛歐補償基金」(pan-EU compensation fund)的緣故,是故目前主要由設有VICP的成員國各自設置補償基金。[41]以前述16個歐洲國家為例,僅有丹麥、芬蘭、法國、德國、意大利、拉脫維亞、挪威、瑞典、瑞士以及英國的10國有指定基金之專屬資金來源:有的國家是由財政部編列預算(例如丹麥、法國和意大利);有的國家是以特別稅項支應(例如芬蘭);有的國家是以各邦一般收入來因應(例如德國);有的國家的基金是來源於醫療機構(例如拉脫維亞);有的國家是以國家財政搭配製藥公司提撥的營收組成(例如挪威);有的國家是以藥商年銷售額的百分比作為基金來源(例如瑞典);最後,乃由聯邦政府支應的(瑞士)以及由政府資助的(英國)。[42]
由此可見,除經內國法程序的相關歐盟指令外,該計劃在歐盟成員國間差異極大。舉補償基金的資金來源為例,有的歐洲國家乃以是否為一次性付款,即指基於醫療費用、收入損失而來之貨幣補償(monetary redress);也有國家是以非貨幣為標準的貨幣補償(monetary compensation based on non-monetary criteria),例如精神上的損害賠償。然而,值得一提的是,大多數的資金來源,均源自於由各國中央政府直接或間接的資助。
第五節 以新加坡為例探討接種新冠疫苗後不良反應之救濟機制
范國華/主持律師、吳尊傑/法務助理
截止2021年11月22日,新加坡分別接種第一、二劑疫苗的人口比例為86%和85%,完全接種人口佔合資格人口的94%。[43]如今,總人口570萬的新加坡疫苗全民覆蓋率已逼近九成,也就是說已經跨過群體免疫7-8成的門檻。值得一提的是,輝瑞BNT新冠疫苗於2020年12月 30日推出使用,緊接著的是在2021年3月12日推出 Moderna新冠疫苗。惟截至2021年6月30日,新加坡衛生科學局(Health Sciences Authority,下稱「HSA」)已收到6,606份與使用輝瑞BNT疫苗以及Moderna疫苗相關的疑似不良事件(adverse events,下稱「AEs」)報告,該擬似不良事件占全部接種劑量的0.12%。其中大約73%的AEs發生在60歲以下的群體中。值得注意的是,在前述兩種疫苗的臨床試驗中,60歲以下比60歲及以上的人更容易發生反應原性AEs(reactogenic AEs)。基於年輕的個體具有更活躍的免疫反應,故這是身體對新冠病毒感染建立免疫力的自然反應的一部分。又大約64%的AEs是發生在女性群體中。[44]有鑑於此,新加坡政府設置了「針對新冠疫苗接種的疫苗傷害財務援助計劃」(Vaccine Injury Financial Assistance Programme for COVID-19 Vaccination,下稱「VIFAP」)。[45]據報導,截至2021年5月3日,已有104宗個案聲稱因接種後產生嚴重不良副作用,故向新加坡衛生部提出申請;但卻僅有30人符合經濟補償的資格。[46]本文以下將從新加坡的VIFAP財務補償制度中進行說明、討論。
新加坡政府為了保護國民免受新冠病毒感染及其可能帶來的嚴重健康後果,所有永久和非永久性居民都可以免費接種新冠疫苗。目前新加坡使用的疫苗已被HSA及新冠疫苗接種專家委員會評估為安全有效。縱然如此,但在極少數情況下,人們可能會出現嚴重的副作用(例如嚴重的過敏反應)。基此,當局推出了VIFAP計劃,以便於為經歷嚴重副作用的人提供「一次性善意的財務援助」(one-time goodwill financial assistance),惟前提是該副作用經評估與在新加坡接種的新冠疫苗有關。要成為VIFAP計劃申請人的資格,本人必須是新加坡公民、永久居民或長期通行證的持有人,如果他們在新加坡接種了疫苗,並經歷了可能危及生命或致命性副作用,或需要住院治療或導致持續喪失工作能力甚至乎殘疾的情況,仍須由醫師評估與個人接種的新冠疫苗有關。總而言之,VIFAP將使接種疫苗的人更加安心,如此即有助於當局提高新冠疫苗接種之全民覆蓋率。[47]
誰可以申請VIFAP?
經建議接種通過HSA授權用於「大流行特殊通道」(Pandemic Special Access Route,下稱「PSAR」)或依據《新加坡健康產品法》註冊的新冠疫苗之新加坡公民、永久居民或長期通行證持有人,若經醫師評估其招致之嚴重副作用乃與新加坡授權之疫苗接種有關,則得申請VIFAP。
合於接種後產生嚴重副作用之VIFAP補償條件
嚴重副作用是潛在危及性命的風險、並且需要住院照護或將導致持續的干擾或殘疾。一旦接種者有發生前述嚴重副作用時,則得申請財務援助。所有申請將由一個獨立的臨床小組審查,以便對該疫苗產生的副作用及其嚴重程度和相關性進行調查。
提供多少財務援助?會否全額支付歸因於嚴重副作用的醫療費用?
| 嚴重副作用的類型 | 一次性支付金額 |
| 導致死亡或永久性嚴重殘疾 | 225,000新加坡幣 (約相當於新臺幣4,619,688元) |
| 需要接受高度的重症醫療照護,並隨後恢復 | 10,000新加坡幣 (約相當於新臺幣205,319元) |
| 需要接受住院治療及醫療干預,並隨後恢復(不包括無需隨後入院治療的AE事件) | 2,000 新加坡幣 (約相當於新臺幣41,064元) |
資料來源:新加坡衛生部
VIFAP是一種獨立於現有醫療融資和保險計劃的善意財務援助計劃。若當事人患有由疫苗造成的嚴重副作用,則VIFAP為患者提供了額外的財務支持。但VIFAP並不意味著清償與嚴重副作用相關的醫療費用。在新冠疫苗接種後產生副作用的個人,可以通過適用的醫療保健融資計劃(healthcare financing schemes)繼續獲得支持,包括Medishiff Life和公共衛生醫療機構等提供的補貼。另外,若有投保私人保險的人,則希望能在其承保範圍內與保險業者聯繫。
怎樣申請、處理、何時通知及若發生醫療情況惡化情況…?
通過在線申請VIFAP。所有申請必須通過醫師的評估。作為提交的一部分,申請人必須提供由其主診醫師完成的「醫療資訊請求」表格(Request for Medical Information)。由主診醫師填寫完畢後並返還於申請人。前述表格,主診醫師已獲告知不應收取任何費用。申請至遲在嚴重副作用發生日後3年內提交。對於21歲以下的人,申請必須由父母或法律監護人提交。對於殘疾人或身亡者,該申請可以由接種者的近親、遺體受贈者、代理人或管理人員提交。
當有權機構收到在線申請所需之所有申請文件(包括申請表、身份證明以及醫療資訊請求表)時,爾後處理時間約需時一個月。然而,嚴重副作用的複雜性和提交申請的完整性,亦可能影響該處理時間。
最後,由新加坡衛生部(the Ministry of Health,下稱「MOH」)指定的獨立臨床小組審查並評估個人提出的申請,以確定其是否有資格獲得幫助。不論是否獲得補償,MOH皆通過電子郵件或郵寄來通知正式的結果。對於成功的申請者而言,MOH將透過必要的紙本流程與申請人聯繫以處理後續指定銀行賬戶匯款之作業。不過,若當事人在收到給付後出現嚴重副作用下之醫療惡化結果,則依前述流程,得重新提交由主診醫師填寫之「醫療資訊請求單」,以便重新評估及後續程序之再進行。
經「特殊通道」(SAR)進來的新冠疫苗[48]
不過,新加坡衛生部為了提高人民選擇疫苗的彈性,將通過允許私人醫療機構在特殊通道 ( Special Access Route,下稱「SAR」 ) 下申請其他疫苗之進口、使用。SAR允許進口和供應未經註冊之世界衛生組織批准列入其緊急使用清單(Emergency Use Listing,下稱「EUL」)的藥物,以滿足潛在的醫療需求。基此,如果選擇接種該經SAR通道進口的疫苗者,應先與其醫師進行討論,並作出知情的決定(informed decision)。除此之外,尚需簽署知情同意書(informed consent form),以承諾其將承擔所有風險。因此,接種此類疫苗的人,將沒有資格參加VIFAP計劃。
綜上所述,除了經私人醫療機構申請在SAR管道下進口使用之疫苗外,接種兩款已獲MOH授權使用之新冠疫苗者(下稱「第一類人」),若有任何嚴重副作用,第一類人得依上述程序申請VIFAP的財務援助。相反,若是接種自SAR進口的疫苗(下稱「第二類人」),則排除適用VIFAP的餘地。由此可見,新加坡對前揭第一類人採取較積極的救濟指導,相對於第一類人的第二類人,縱然政府採取較為消極之救濟指導。惟仍需依《新加坡健康產品法》第2(a)條規定之一項或多項條件,即在提出申請之前,合資格醫療機構或公司須進入申請前的諮詢程序(需先通知HAS),以便進行諮詢程序以討論相關數據提交計劃,後續則以「滾動式」的方式來提交數據。[49]
第六節 以台灣法為中心初探完善新冠疫苗的疫害救濟之方向
范國華/主持律師、吳尊傑/法務助理
最近,新冠肆虐台灣;三級警戒持續至今,已將近二月有餘。惟值得關注的是,截至2021年7月21日下午6時為止,因疫苗不良反應而致死者計有481例;其中若按年齡分布,65歲以上、50至64歲和18至49歲者依序為427、41以及12例。[50]然而,需先對預防接種的「不良事件」及「不良反應」進行釐清,前者是指「在預防接種後所發生任何對健康造成負面影響的事件,然而該事件未必與預防接種有因果關係。」至於後者,則是指「接種疫苗後所發生之有害且與接種疫苗具有合理因果關係之反應。」簡單來說,後者相較於前者,其產生的不良反應多具有因果關係。[51]本文以下先就疫苗取得緊急使用授權或依通常程序來取得藥證之相同和不同點進行討論。
一般而言,新藥取得藥證之管道,依藥事法第三十九條第一項規定,製造或輸入藥品,應將其成分、原料藥來源、規格、性能和製法之主要內容,檢驗規格與方法及有關資料或證件,連同原文和中文標籤、原文和中文仿單及樣品,並繳納費用,申請衛福部查驗登記,經核准發給藥品許可證後,始得製造或輸入。而在經衛福部查驗登記及核發許可證前,皆需以四期臨床試驗為原則,若藥物在第三期臨床過程中被證實藥物療效,即可申請新藥上市許可;具體而言,依序以通過一期的人體藥理研究(安全性)、二期的治療探索(兼具安全性的療效)、三期的治療確認(證實療效及安全性)以及四期的治療使用(藥品上市後的追蹤)為原則。[52]但在新冠疫情持續延燒下,關於自產疫苗或授予外國疫苗境內之緊急使用授權,衛福部係依據同法第四十八條之二規定,得以專案核准特定藥物之製造或輸入;至於該專案核准之申請條件、審查程序、核准基準等有關事實,由衛福部另外訂定,不受同法第三十九條及四十條之限制。[53]換言之,緊急使用授權下的新藥上市或輸入,差異僅在於加快境內外新藥之儘速上市(例如臺灣是以二期期中數據通過高端疫苗之EUA;而國外則以三期期中數據通過EUA)。故以下將就兩者在藥害(不良反應)救濟上進行討論。
關於受種者的疫害補償請求權。不管是獲緊急使用授權之新藥或經一般新藥核准上市程序,皆需依傳染病防制法第三十條的規定,由衛生福利部在疫苗受檢驗及格時,向藥商徵收一定金額充作預防接種受害救濟基金;至於徵收之金額、繳交期限、免徵範圍與預防接種受害救濟之資格、給付種類、金額、審議方式、程序以及其他應遵行事項的辦法,由衛福部另定「預防接種受害救濟基金徵收及審議辦法」(下稱「徵收及審議辦法」)執行之。所以,因接種新冠病毒疫苗而受害者,自受害人知有受害事實之日起,可以請求救濟補償;但如果兩年間不行使該請求權,則意味該請求權消滅。縱使受害人不知有前述情事,惟自受害發生日起,超過五年者亦歸消滅。
在實務上,該疑似因接種新冠疫苗後受害之人可以填寫申請書、並提出受害資料於接種地衛生局。衛生局在接到受害個案後,將進行調查及整備相關資料;後再由衛福部之委辦單位—社團法人國家生技醫療產業策進會(下稱「生策會」)進行審議準備工作。待工作完成後由衛福部召開「預防接種受害救濟審議小組會議」,審議結果若認為受害人是符合救濟條件者,即以書面通知其具領據資料提交於接種地衛生局,由其撥付救濟金於領款人。相反,則以不符合救濟條件為理由作出不予給付之處分,個案至此告終。[54]因此,在臺灣接種新冠疫苗後發生嚴重不良反應乃比照常規疫苗預防接種受害救濟機制,最高給付為新台幣六百萬元。[55]
再依前述徵收及審議辦法規定,受害者是指本人因預防接種由衛福部核發許可證或以專案核准進口之疫苗而受害的人。[56]基此,不管是疫苗製造商或是核准專案進口商,皆應在衛福部核准上市許可後次日起三十日內,按每一劑疫苗徵收新臺幣1.5元來繳納徵收金至「預防接種受害救濟基金」(下稱「基金」);惟若基金總額未達新臺幣一億五千萬元或超過四億元時,衛福部就可以依基金收支運用情形調整之。[57]基金得對以下四類人進行受害救濟給付:(1)由疑似受害人的法定繼承人申請的死亡給付;(2)疑似受害人申請的障礙給付;(3)疑似受害人申請的嚴重疾病給付;以及(4)因疑似受害人之其他不良反應申請的給付。[58]唯上述皆需經審議小組就預防接種與受害情形是否具有關聯性進行綜合研判(包括受害人接種前後之病史、家族病史、過去接種類似疫苗後之反應、藥物使用、毒素暴露、生物學上之贊同性及其他相關因素)後作出專業的醫療判斷。[59]
換言之,決定你是否能獲得疫害救濟的關鍵,就在於「疫害結果」與「接種原因」之間須具備「相關性」。否則,一旦有以下情況者:(1)發生死亡、障礙、嚴重疾病或其他不良反應與預防接種確定無關;(2)常見、輕微之可預期預防接種不良反應;(3)轉化症或其他因心理因素所致之障礙;和(4)非因預防接種目的使用疫苗致生損害,就不予救濟。[60]惟,經認定為與預防接種之關聯性係介於相關和無法確定的話,則給付金額範圍如下表所示:[61]
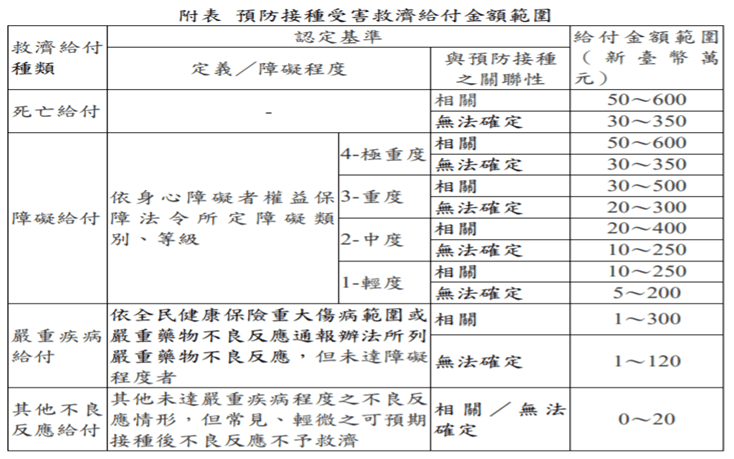
第十八條附表修正規定
最後,關於相關性的判斷,除了基於前述判斷基準外,或有適用實務上行之有年的疫學上因果關係的餘地。所謂「疫學上因果關係」,依晚近最高法院的判決,乃指「利用統計方法,以『合理之蓋然性』為基礎,即使不能證明被告之行為確實造成原告目前損害,但在統計上,被告之行為所增加之危險已達『醫學上合理確定性』,即推定因果關係之存在,主要為適用於公害事件之特殊性。」但法院卻認為,由於上訴人未就其罹患病症與接種流感疫苗是否有疫學上因果關係存在,提出相關統計數字以證明「醫學上合理確定性」存在,因此認為上訴人未盡相關舉證責任而不得請求救濟。[62]由此可見,要受害人舉證證明(提出受害資料)彼此間乃存在相關性或因果關係,是何其的困難?!
總而言之,在通常情況下,受害者得依藥害救濟法第四條第一項的規定,因正當使用合法藥物所生藥害,可以依法請求救濟。故有學者認為這相當於一種「無過失責任」,因此救濟金額一來不可能設有上限,二來也不可能是完全的補償。[63]加之,若有事實足以認定藥害之產生應由藥害受害人、藥物製造業者或輸入業者、醫師或其他之人負其責任,那麼就不可以申請藥害救濟。[64]也就是說,國家僅在無法彌補或難以求得損害賠償時承擔救濟責任。
然而,時值新冠大疫(COVID-19)盛行全球,是故除了需減輕受害人之舉證負擔外,更需對疫苗緊急使用授權之製造商或經核准輸入者於以免責(目前並未見政府出台相關製造商免責的規定);又,設置專屬新冠疫害救濟基金(或可以特別公課挹注之),並由國家承擔最終之補償責任等,希冀作為當局未來完善相關新冠疫害救濟機制的方向。
相關出版聲明
免責聲明(Disclaimer)
本期報告是針對一般性議題彙整相關資訊,並非針對特定個案表示任何專業意見,閱讀本期報告者不宜在未取得特定專業意見下,直接採用本期報告之任何資訊。「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」,包括其管理當局(合夥人)、員工及所委任之顧問,不對本期報告資訊的正確及完整與否負任何保證責任,亦不對本期報告承擔任何義務或責任。閱讀本期報告者因使用本期報告資訊所引發之任何損失、損害或任何性質之費用,「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」亦不負任何責任。
智財權聲明(Copyright Disclaimer)
本刊物是由「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」製作並擁有著作權。本刊物所有著作內容未經「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」書面同意,請勿修訂或翻印,侵害必究。
授權聲明
本刊物不代表「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」的觀點。文字內容及版式的著作權為「眾律國際法律事務所」、「眾律國際商務數位智權有限公司」和「眾律國際專利商標事務所」所有,需要使用本刊作品之個人、機構或媒體,須先與本刊編輯部門聯繫獲得書面授權。
編輯團隊
眾律國際法律事務所
眾律國際專利商標事務所
眾律國際商務數位智權有限公司
范國華 主持律師/研究主持人員
吳尊傑 法務專員/協同研究人員
毛紹儒 所內專員/平面設計人員
媒體合作
聯絡人:吳尊傑 法務專員 電郵:kitson.wu@zoomlaw.com.tw.
[1] 原文網址: 富國超量掃貨 窮國買嘸疫苗 新冠肺炎重塑全球公衛格局?(范國華、吳尊傑) | 雲論 | ETtoday新聞雲 https://forum.ettoday.net/news/2017802#ixzz7D7FGibN1.
Follow us: @ETtodaynet on Twitter | ETtoday on Facebook
[2] 原文網址: 疫苗採購新加坡快速有效 醫院採購 政府把關 專案核准(范國華、吳尊傑) | 雲論 | ETtoday新聞雲 https://forum.ettoday.net/news/2006199#ixzz7D7rlmGvc.
Follow us: @ETtodaynet on Twitter | ETtoday on Facebook
[3] Timothy Goh, Coronavirus Singapore, ‘MOH gives green light to Sinovac shot under special access route’, 3 June 2021. https://www.straitstimes.com/singapore/health/moh-gives-green-light-to-sinovac-shot-under-special-access-route. Last visited 7 June 2021.
[4] See EU Vaccines Strategy, https://ec.europa.eu/info/live-work-travel-eu/coronavirus-response/public-health/eu-vaccines-strategy_en. Last visited 8 June 2021.
[5] See HSA, ‘Pandemic Special Access Route (PSAR) for Supply of Emergency Therapeutic Products’. https://www.hsa.gov.sg/therapeutic-products/register/special-access-routes/psar-emergency-therapeutic-product. Last visited 7 June 2021.
[6] Id.
[7] See, EU, ‘COVID-19 vaccines: How are they developed, authorised and put on the market?’, December 2020. https://ec.europa.eu/commission/presscorner/detail/en/fs_20_2245. Last visited 8 June 2021.
[8] See, How are vaccines being rolled out in the EU?. https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/vaccines-covid-19/covid-19-vaccines-key-facts#how-are-vaccines-being-rolled-out-in-the-eu?-section. Last visited 9 June 2021.
[9] See EU, COVID-19 vaccines: key facts. https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/vaccines-covid-19/covid-19-vaccines-key-facts. Last visited 9 June 2021.
[10] See Reuters, Kate Kelland, ‘WHO agrees compensation fund for serious COVAX vaccine side effects’, 23 February 2021. https://www.reuters.com/article/uk-health-coronavirus-who-vaccines-compe-idUSKBN2AN0GV. Last Visited 13 July 2021.
[11] See WHO News Release, No-fault compensation programme for COVID-19 vaccines is a world first, 22 February 2021. https://www.who.int/news/item/22-02-2021-no-fault-compensation-programme-for-covid-19-vaccines-is-a-world-first. Last Visited 13 July 2021.
[12] WHO, Emergency Use Listing Procedure, 7-8 (Version 13 December 2020). https://cdn.who.int/media/docs/default-source/medicines/eulprocedure_a63b659c-1cdc-4cee-aa2d-ef5dd9d94f0b.pdf?sfvrsn=55fe3ab8_7&download=true. Last Visited 13 July 2021.
[13] Id at 9.
[14] Id at 19.
[15] OECD Policy Responses to Coronavirus (COVID-19), ‘Enhancing public trust in COVID-19 vaccination: The role of governments’, 10 May 2021. https://www.oecd.org/coronavirus/policy-responses/enhancing-public-trust-in-covid-19-vaccination-the-role-of-governments-eae0ec5a/. Last Visited 13 July 2021.
[16] 參見澳門新聞局,記者會快訊(本澳接種新冠疫苗數據),2021年07月16日。https://www.gov.mo/zh-hant/news/603408/。最後瀏覽日:2021年07月22日。
[17] 參見香港新冠疫苗的安全監察,2021年06月30日。https://www.drugoffice.gov.hk/eps/do/tc/doc/Safety_Monitoring_of_COVID-19_Vaccines_in_Hong_Kong.pdf。最後瀏覽日:2021年07月22日。
[18] 參見衛健委,新冠病毒疫苗接种情况,2021年11月23日。http://www.nhc.gov.cn/jkj/s7915/202111/e3117afc766e48ca925f4137c13bafff.shtml。 最後瀏覽日:2021年11月24日。
[19] 參見環球時報,「自信!中國疾控中心首次發布我國新冠疫苗接種不良反應監測情況」,2021年05月28日。https://finance.sina.com.cn/tech/2021-05-28/doc-ikmyaawc8112553.shtml。最後瀏覽日:2021年07月22日。
[20] 參見澳門「第27/2021號行政長官批示」。https://images.io.gov.mo/bo/i/2021/09/despce-27-2021.pdf。最後瀏覽日:2021年07月23日。
[21] 參見《澳門防疫接種制度》第4條第一項。
[22] 關於忠誠澳門新型冠状病毒疫苗保險」,請參見https://www.fidelidade.com.mo/zh-hant/contact-us/covid-19-vaccine-insurance/。最後瀏覽日:2021年07月23日。
[23] 參見澳門抗疫專頁。https://www.ssm.gov.mo/apps1/PreventCOVID-19/ch.aspx#clg17458。最後瀏覽日:2021年07月23日。
[24] 參見香港新冠疫苗專頁。https://www.covidvaccine.gov.hk/zh-HK/vaccine。最後瀏覽日:2021年07月23日。
[25] 同上註。
[26] 參見「為接種2019冠狀病毒病疫苗後出現的異常事件設立的保障基金」。https://www.covidvaccine.gov.hk/zh-HK/AEFI_Fund。最後瀏覽日:2021年07月23日。
[27] 參見中國新聞網,「國家衛健委官員:下一步考慮適度擴大新冠疫苗緊急使用的範圍」,2020年08月23日。http://www.chinanews.com/gn/2020/08-23/9272024.shtml。最後瀏覽日:2021年07月23日。
[28] 參見疫苗責任強制保險管理辦法徵求意見稿第2條。
[29] 同前註第9條。
[30] 參同前註,第13、14條。
[31] 參見中國銀行保險報,「接种新冠病毒疫苗有异常反应也能赔?怎么赔?」,2021年04月09日。https://mp.weixin.qq.com/s?search_click_id=5517891589659908219-1626951646934-513936&sub&__biz=MjM5Nzc4MzQ4Mw==&mid=2653414131&idx=2&sn=1d826d1b9d884efa4210a642dc25e3df&chksm=bd07f0278a707931d950f3e00a95a52f5353e6778cf0191b010ca769e186670d5ee3c2765a1e&&scene=11&subscene=10000&clicktime=1626951646&enterid=1626951646#rd。最後瀏覽日:2021年07月23日。
[32] See COVID-19 Vaccinations in the United States, CDC, https://covid.cdc.gov/covid-data-tracker/#vaccinations. Last visited 15 July 2021.
[33] See John Lauerman & Jason Gale, What to Know About Blood Clots, Anaphylaxis and Other Vaccine Fears, Bloomberg (Jan. 18, 2021; updated April 13, 2021), https://tinyurl.com/2uuxuytj. Last Visited 15 July 2021.
[34] Laurel Wamsley, U.S. Lifts Pause in Use of J&J Vaccine After Vote by Expert Panel, NPR (Apr. 23, 2021), https://tinyurl.com/cvuza44e. Last Visited 15 July 2021.
[35] National Vaccine Injury Compensation Program, https://www.hrsa.gov/vaccine-compensation/index.html. Last Visited 15 July 2021.
[36] Congressional research service, The PREP Act and COVID-19: Limiting Liability for Medical Countermeasures, 19 March 2021, 1-4. https://crsreports.congress.gov/product/pdf/LSB/LSB10443. Last Visited 16 July 2021.
[37] Jessica Doyle and Eoin McLoughlin, Vaccine Injury Compensation Programmes: An Overview, Library & Research Service, 20 April 2021. https://data.oireachtas.ie/ie/oireachtas/libraryResearch/2021/2021-04-20_l-rs-note-vaccine-injury-compensation-programmes-an-overview_en.pdf. Last Visited 19 July 2021.
[38] Directive 2001/83/EC of The European Parliament and Of the Council of 6 November 2001 on the Community code relating to medicinal products for human use (OJ L 311, 28.11.2001, p. 67).
[39] Directive 85/374/EEC – liability for defective products.
[40] Id 1, at 0-1.
[41] Arnold & Porter Kaye Scholer LLP, Worldwide: Major Market Comparison Of Key COVID-19 Legislation, 15 March 2021. https://www.mondaq.com/unitedstates/antitrust-eu-competition-/1046630/major-market-comparison-of-key-covid-19-legislation. Last Visited 19 July 2021.
[42] Id 1, at 5-8.
[43] See, Vaccination Data (as of 18 Jul 2021). https://www.moh.gov.sg/covid-19/vaccination. Last Visited 20 July 2021.
[44] See, HSA’s Safety Update #3 Pfizer-BioNTech and Moderna COVID-19 Vaccines (30 December 2020 – 30 June 2021). https://www.hsa.gov.sg/docs/default-source/hprg-vcb/safety-update-on-covid19-vaccines/hsa-safety-update-no-3-on-covid-19-vaccines-(30-june-2021).pdf. Last Visited 20 July 2021.
[45] See, Vaccine Injury Financial Assistance Programme for COVID-19 Vaccination (VIFAP). https://www.moh.gov.sg/covid-19/vaccination/vifap. Last Visited 20 July 2021.
[46] Rei Kurohi, ‘30 who had serious Covid-19 vaccine side effects in S’pore to get financial help’, 11 May 2021. https://www.straitstimes.com/singapore/politics/30-patients-who-experienced-serious-covid-19-vaccine-side-effects-to-get. Last Visited 20 July 2021.
[47] See Id, at 3.
[48] See, Singapore Government, ‘Expanding Singapore’s vaccination programme’, 31 May 2021. https://www.gov.sg/article/expanding-singapores-vaccination-programme. Last Visited 21 July 2021.
[49] 參見「疫苗採購新加坡快速有效 醫院採購 政府把關 專案核准(范國華、吳尊傑) 」| 雲論 | ETtoday新聞雲 https://forum.ettoday.net/news/2006199#ixzz71F79fHyM。最後瀏覽日:2021年07月21日。
[50] 參見中央流行疫情指揮中心的簡報,「COVID-19疫苗安全性監測」,資料整理日:2021年07月27日。https://www.cdc.gov.tw/File/Get/mWej1OcmFIqxijlxtBAcmA。最後瀏覽日:2021年07月28日。
[51] 林詠青,焦點特寫,「COVID-19 疫苗系列專欄:什麼是預防接種的不良事件和不良反應?」,2021年5月25日,頁146。https://www.cdc.gov.tw/File/Get/PTm0uLhIccDsOUhoywksjg。最後瀏覽日:2021年07月26日。
[52] 參見長庚醫院,「臨床試驗介紹」, https://www1.cgmh.org.tw/intr/intr2/c3s400/introduction.html。最後瀏覽日:2021年07月28日。
[53] 參見藥事法第48條之2。
[54] 參見申請流程,https://www.cdc.gov.tw/File/Get/VbbNaufONKNDFr4NL24Lxw。最後瀏覽日:2021年07月27日。
[55] 參見國家生技醫療產業策進會,「新冠疫苗副作用25國設補償機制,台最高給付600萬」,2021年02月25日。https://ibmi.taiwan-healthcare.org/news_detail.php?REFDOCTYPID=0o4dd9ctwhtyumw0&REFDOCID=0qp289lbwo03jgol&PageNO=1。最後瀏覽日:2021年07月28日。
[56] 預防接種受害救濟基金徵收及審議辦法第2條。
[57] 預防接種受害救濟基金徵收及審議辦法第3、4條。
[58] 預防接種受害救濟基金徵收及審議辦法第5條。
[59] 預防接種受害救濟基金徵收及審議辦法第13條。
[60] 預防接種受害救濟基金徵收及審議辦法第17條。
[61] 參見「第十八條附表修正規定」,https://law.moj.gov.tw/LawClass/LawGetFile.ashx?FileId=0000287042&lan=C。最後瀏覽日:2021年07月27日。
[62] 參見最高法院 102 年台上字第 31 號民事判決。
[63] 參見原文網址: 吳景欽/疫苗副作用製造者要負賠償責任嗎 | ETtoday法律新聞 | ETtoday新聞雲 https://www.ettoday.net/news/20210617/2000838.htm#ixzz71p0e4IpN。最後瀏覽日:2021年07月27日。
[64] 參見藥害救濟法第13條第1項第1款。